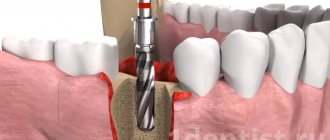
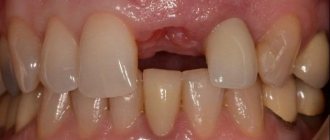
Корни наших зубов находятся в костной ткани челюсти. Благодаря тому, что во время пережевывания пищи кость получает нагрузку от зубов, она полноценно функционирует, насыщается питательными веществами. Но как только зуб удаляется, на его месте образуется пустое пространство – клетки кости растут достаточно медленно и не успевают заполнить это место. В результате кость уменьшается в размерах, к тому же обменные процессы нарушаются и клетки перестают получать кислород и питательные вещества. Кость атрофируется.
Атрофия костной ткани является большой проблемой при отсутствии большого количества зубов. Ведь в этом случае возникают не только эстетические и психологические проблемы (кожа лица обвисает, появляются морщины возле губ, щеки проваливаются, губы становятся более тонкими и западают внутрь полости рта), но и функциональные – ведь питаться при отсутствии зубов вряд ли получится полноценно и качественно.
Направленная регенерация костной ткани – это хирургическая операция, цель которой – восстановить объем челюстной кости, то есть нарастить ее до прежних размеров, заложенных природой. Данная операция в основном проводится как подготовительный этап перед имплантацией зубов – ведь для того, чтобы вживить и надежно закрепить имплантаты (искусственные металлические корни) требуется достаточный объем прочной кости. Иногда она может проводиться вместе с установкой имплантатов.
Специальные предложения!
Пластика костной ткани, открытый синус-лифтинг — 35 000 руб. Закрытый синус-лифтинг (область 1 зуба, без учета стоимости костного заменителя) — 10 000 руб. Направленная регенерация костной ткани (область 1 зуб) — 10 000 руб. Направленная регенерация костной ткани (НРК) — 35 000 руб.
Материалы для наращивания костной ткани
Само слово «регенерация» в переводе с латинского означает «возрождение» или «возобновление». Операция проводится хирургическим путем и суть ее сводится к подсадке костного материала в область, где объема челюстной кости недостаточно.
Для регенерации костной ткани могут применяться различные материалы:
- собственная кость пациента: самый предпочтительный вариант, поскольку в этом случае достигается 100% результат приживления материала. Кусочек кости заимствуется, как правило, из области подбородка, угла нижней челюсти (где расположены самые дальние зубы мудрости) или тазобедренной области. Явный недостаток в том, что часто приходится проводить два хирургических вмешательства одновременно,
- искусственные синтетические материалы: разработаны в лабораторных условиях. Довольно распространенный вариант, сегодня используется повсеместно, в большинстве случаев в качестве дополнительного материала при подсадке собственной кости пациента. Отличается хорошей приживаемостью,
- родственная кость: как правило, это очищенная трупная кость другого человека, которая находится в стерильной банке. Также хорошо приживается, при этом не требуется дополнительное хирургическое вмешательство,
- кость животного: материал может быть представлен в виде костных блоков или в виде стружки. Хорошо приживается и почти не отторгается.
Регенерация кости: как проводится?
Операция длится 1-2 часа, в зависимости от объема и сложности работ. Через 3-4 месяца, когда подсаженный кусочек срастется с натуральной костью, можно будет переходить к установке имплантатов. В некоторых случаях может потребоваться больше времени на приживление, в зависимости от индивидуальных особенностей организма. Технология проведения регенерации костной ткани следующая:
- вводится анестезия, в некоторых случаях, если требуется серьезное хирургическое вмешательство возможно проведение операции под наркозом,
- создается доступ к кости: надрезается и отслаивается кусочек десны, при помощи защитных мембран, которые со временем самостоятельно рассасываются, формируется полость для заполнения костной стружкой,
- вводится костный материал: полость заполняется искусственным или натуральным костным материалом. Через 2-4 месяца клетки натуральной кости проникнут вглубь подсаженного материала, и он превратиться в собственную костную ткань – тогда можно будет приступать к имплантации. Сверху новая кость прикрывается защитной мембраной, которая будет защищать от давления со стороны десны,
- десна ушивается – на слизистой фиксируются швы, которые снимаются в среднем через неделю.
Мнение специалиста
Эмир Романович Омерэлли
Челюстно-лицевой хирург, имплантолог
Стаж: более 13 лет
Если по результатам обследования врач диагностирует недостаток костной ткани, необходимо обязательно нарастить ее объем перед проведением имплантации. Установка имплантов в низкую или узкую кость сопряжена с серьезными рисками. Кость может расколоться, или сам имплант выпадет после непродолжительного использования. Чтобы этого не случилось перед классической имплантацией верхних зубов необходимо провести синус-лифтинг, для нижних – наращивание посредством остеопластики. Исключением является только базальный протокол, согласно которому импланты можно устанавливать без костной пластики и без рисков.
Если костной ткани не хватает по ширине, то есть она очень тонкая, операция может проводиться путем расщепления альвеолярного гребня: сначала отслаивается десна, затем кость по длине разрезается и внутрь помещается искусственный или натуральный костный материал.
Также проблема узкой костной ткани решается подсадкой костного блока, позаимствованного из другой кости самого пациента. Для этого кусочек кости помещается под десну, фиксируется на специальные винты, вокруг посыпается костной стружкой, прикрывается барьерной мембраной и десной – слизистая ушивается. Такой вариант более предпочтительный, поскольку собственная кость в большинстве случаев приживается.
Операция по наращиванию костной ткани в зависимости от показаний может проводиться одновременно с установкой классических имплантатов без их последующей нагрузки. То есть искусственные корни фиксируются в кости, но прикрываются десной – протезы будут зафиксированы через 3-4 месяца. Для того, чтобы классические имплантаты прижились в кости необходимо обеспечить их покой и избавить от любого давления.
Осложнения после регенерации костной ткани
Операция наращивания костной ткани считается одной из самых безопасных в стоматологии, сложных, но при грамотном проведении – без каких-либо неприятных последствий. В первые дни после операции уже становится ясно – приживается блок или операцию придется провести заново. Из неприятных ощущений – небольшие отеки тканей и боли в области забора костного блока и места его пересадки. Но через 2-4 дня все неприятные ощущения проходят самостоятельно.
После наращивания костной ткани
После процедуры регенерации кости пациенту необходимо соблюдать меры предосторожности: обязательно пить лекарственные препараты, назначенные врачом – для быстрого восстановления организма, не игнорировать обезболивающие средства. В течение 2-3 часов после операции стоит отказаться от приема пищи, после она должна быть теплой, но не слишком холодной или горячей. Пережевывать продукты рекомендуется на противоположной от хирургического вмешательства стороне. Кроме того, на время необходимо отказаться от физических нагрузок и пару дней после операции обеспечить организму покой. Не забудьте посетить своего лечащего врача для профилактического осмотра и контроля результатов лечения.
Другие работы
В настоящее время травматизм входит в пятерку ведущих смертности в мире, угрожая экономическому и социальному развитию. Переломы длинных костей занимают ведущее место в структуре травматизма последних десятилетий и составляют, по данным различных авторов, составляют до 80% всех повреждений костей скелета.
Поэтому проблема лечения переломов костей последние годы сохраняет актуальность, хотя прогресс в области травматологии является несомненным. Остается нерешенным ряд вопросов, связанных с так называемой остеогенной недостаточностью.
Несмотря на применение современных медицинских технологий, процент осложнений, возникающих в результате лечения переломов длинных костей, остается высоким.
К ним относятся замедленная консолидация, формирование ложных суставов, несращение костных отломков и другие проблемы.
Так, нарушение консолидации костных отломков при переломах длинных костей составляет от 15 до 50%, а частота ложных суставов варьирует от 4 до 33%.
Согласно данным Американской ассоциации ортопедии, из двух миллионов переломов длинных костей в США ежегодно около 100 тысяч завершаются несращением.
По информации отечественных исследователей, нарушения консолидации костных отломков при переломах костей конечностей составляют около 25% в структуре инвалидности пострадавших от механической травмы.
Процент неудач в процессе лечении подобных нарушений классическими методами достигает 33%, что почти в два раза превышает число неудовлетворительных анатомо-функциональных результатов лечения переломов.
За последние годы отмечается и скрытый рост инвалидности вследствие травм и увеличения срока консолидации в каждом третьем случае.
Проблема лечения нарушений репаративной регенерации костной ткани, возникающих после диафизарных переломов костей, остается актуальной для современной ортопедии и травматологии. Случаи развития такой патологии составляют от 2,5 до 18%.
В структуре последствий травм длинных костей псевдоартрозы бедренной кости составляют 10-30%, костей голени — 15-50%, плечевой кости — 1-10%.
Обращает на себя внимание, что среди контингента с нарушениями репаративной регенерации костей преобладают лица трудоспособного возраста.
Данная патология отмечается стойкой утратой трудоспособности у 5 человек на 10000 населения, а образованные при этом анатомо-функциональные нарушения конечности являются причиной стойкой инвалидности в 12-45% больных.
Длительное лечение больных с большими материальными затратами, низкая эффективность, высокий уровень инвалидности позволяют считать осложнения при переломах длинных костей важнейшей социальной проблемой, с которой многим пострадавшим сложно справиться без социальной помощи.
Из этого следует, что лечение переломов длинных костей, осложненных репаративными нарушениями, является актуальной экономической и медико-социальной проблемой.
Основная задача современной травматологии заключается в совершенствовании существующих и разработке новых, экономичных и эффективных методов лечения.
Что такое регенерация костной ткани?
Кость представляет собой сложный орган, который выполняет механические и биологические функции в организме и имеет сложную иерархическую структуру.
Кости участвуют в обменных процессах благодаря содержанию значительного процента минеральных веществ организма, а также создают специфическое микроокружение для предшественников крови красного костного мозга.
Костная ткань являет собой динамическую систему, в которой в течение жизни организма происходят два взаимосвязанных противоположных процесса, составляющих природный цикл ремоделирования – резорбция (разрушение) и остеогенез (синтез).
Поэтому условия репаративного остеогенеза постоянно находятся в поле зрения практикующих врачей – травматологов и ортопедов.
Давно известно, что переломы в области компактной (кортикальной) и губчатой (трабекулярной) костной ткани отличаются сроками консолидации, что связано с особенностями ее структурной организации.
Перспектива заживления переломов губчатой кости более благоприятные, поскольку в структуре ее находятся элементы, необходимые для формирования регенерата. В свою очередь, компактная костная ткань характеризуется низкой плотностью сосудов по сравнению с губчатой, а также имеет особенности кровоснабжения.
Репаративная регенерация определяется как процесс восстановления ткани после травмы. Механизмы репаративной и физиологической регенерации одинаковые и основываются на единых биологических закономерностях.
Репаративная регенерация рассматривается как в той или иной степени усиленная физиологическая. Репаративная регенерации костной ткани – она же репаративный остеогенез – важная теоретическая и практическая проблема травматологии.
Действительно, в идеале консолидация перелома должна привести к образованию обновленной костной ткани, идентичной старой, существовавшей до травмы. Однако сращение перелома на практике является достаточно сложным, длительным многостадийным процессом, на который влияет множество факторов.
Кость имеет очень высокий репаративный потенциал.
Проблема состоит в том, что процессы репаративного остеогенеза возможно ускорить за счет активации обмена лишь в очень незначительной степени (порядка недель). С другой стороны, замедлить процесс нарушением физиологических условий очень легко, что нередко происходит из-за недостаточного понимания физиологии кости.
Согласно определению Руцкого и Ткаченко, репаративная регенерация – это сложный процесс, вызванный разрушением костных структур, который количественно превышает допустимые пределы физиологической регенерации и направлен на полное восстановление анатомической целостности и функции кости.
По мнению исследователя А. Корж, процессы регенерации кости являются сложным переплетением общих воздействий на системном уровне и локальных изменений тканевых обменных процессов, включая изменения на молекулярном уровне.
Д. Саркисов и соавторы представляют репаративный остеогенез как физиологическую регенерацию, которая протекает в условиях экстремальных воздействий на организм и отличается большей интенсивностью проявлений.
Другие же исследователи утверждают, что, в отличие от физиологической регенерации, которая фактически является адаптацией, репаративный остеогенез – компенсаторный процесс, восстанавливающий строение после гибели части или всего органа.
Репаративная регенерация каждого типа тканей имеет уникальные особенности, но всегда включает следующие процессы:
- Разрушение поврежденных клеток и структур
- Пролиферация жизнеспособных клеток в области дефекта
- Дифференцировка жизнеспособных клеток регенерата
- Формирование межклеточных связей и перестройка регенерата.
Репаративная регенерация костной ткани бывает неполной или полной.
Полная регенерация характеризуется замещением дефекта тканью, которая соответствует старой ткани. О неполной принято говорить в случаях, когда костный дефект замещается соединительной тканью или рубцом.
Репаративный остеогенез – это многокомпонентный процесс, основными этапами которого являются дифференцировка клеток, пролиферация, резорбция погибшей ткани и образование кости с ее ремоделированием, формирование органического внеклеточного матрикса и его минерализация.
Описанные процессы протекают параллельно, но один из них может стать доминирующим на тех или иных стадиях репаративного остеогенеза.
Практика подтверждает, что костная ткань действительно является уникальной, поскольку способна восстанавливать полностью даже большие по длине дефекты.
Причины нарушений репаративной регенерации кости
Известно, что репаративная регенерация костной ткани является сложным, генетически запрограммированным процессом. Стадийно-временные характеристики этого процесса зависят от действия ряда эндогенных и экзогенных факторов.
Течение остеорепаративного процесса связывают с такими факторами:
- Особенности и интенсивность травмы
- Характер повреждения кости и мягких тканей
- Степень посттравматических расстройств периферического кровоснабжения
- Качество оказания первичной и квалифицированной медицинской помощи
- Особенности восстановительного лечения
- Наличием сопутствующей патологии.
Одно из первых мест среди причин, способствующих развитию нарушения репаративного остеогенеза, занимает несвоевременность и неадекватность оказания квалифицированной медицинской помощи.
Экспериментально доказано, что в случаях отсроченной иммобилизации отломков при переломе костей предплечья уже на 3 сутки проявляются признаки нарушения процесса костной репарации с увеличением срока консолидации в 1,5 раза.
Отсроченное сопоставление отломков костей голени за 14 суток приводит к образованию ложного сустава, а при отсутствии стабильной фиксации отломков сроки формирования периостального костного сращения увеличиваются не менее чем в 4 раза.
Дальнейшие экспериментальные исследования показали, что нарушение условий репаративной регенерации в виде отсроченного до 14 суток сопоставления костных отломков приводят к формированию ложного сустава на 50-е сутки.
При медленном заживлении перелома восстановление кости в обычные сроки не происходит, тормозится ремоделирования и созревания костной мозоли.
Как правило, заживление в подобных ситуациях наступает через год и более.
Перелом расценивают как несросшийся, если по истечении 6 месяцев отсутствуют рентгенологические признаки заживления, или когда отсутствует положительная динамика в течение трех месяцев наблюдения.
При несращении перелома наблюдается торможение репаративных процессов и остановка его заживления. Понятие «замедленная консолидация» принято считать относительным, поскольку сроки сращения переломов у каждого больного индивидуальны и зависят от многих факторов.
Условно эти факторы можно разделить на общие и местные.
Общие факторы связаны с общим состоянием организма, сопутствующей соматической патологией, медикаментозной терапией, наличием вредных привычек и тому подобное.
К факторам второй группы относят отсутствие надежной иммобилизации сегмента, недостаточную репозицию, фиксацию и нарушение кровоснабжения костных отломков, травматичность оперативного вмешательства, нарушения тактики лечения, использование массивных металлических имплантатов.
Важным звеном репаративной регенерации является состояние костной ткани на момент травмы, а также эндемическое состояние региона, где проживает травмированное лицо.
В последнее время увеличивается количество исследований относительно влияния неблагоприятных экологических факторов на репаративный остеогенез костной ткани. Отечественными и зарубежными авторами изучалось влияние экологического окружения человека на структуру и метаболизм костной ткани, от которых зависит ход репаративной регенерации.
Клинические исследования демонстрируют, что повышенное потребление фтора сопровождается ломкостью костей, при этом замедляется процесс репаративного остеогенеза и чаще формируются ложные суставы.
После проведения нескольких экспериментов in vitro ученые пришли к выводу о разрушительном действии радиации на костную ткань, которая также замедляет процессы регенерации и увеличивает количество осложнений.
Поэтому при лечении переломов костей необходимо учитывать воздействие неблагоприятных факторов окружающей среды на регенерацию костной ткани.
В настоящее время темой научных дискуссий является вопрос зависимости частоты нарушений остеорепаративных процессов от механизма травмы. Согласно клиническим исследованиям, этиологический фактор травмы влияет на процессы заживления раны.
На течение репаративного процесса влияет как разновидность травмирующего агента, так и характер повреждения костной ткани. По данным ряда авторов, у 55% пациентов с нарушением репаративного остеогенеза травма получена в результате действия высокоэнергетического травмирующего агента.
Проведенные экспериментальные исследования выявили, что при воздействии травмирующей силы высокой интенсивности происходит гибель значительного числа клеточных источников остеорепарации, а сохранившиеся клетки претерпевают настолько значительные морфологических изменения, что не в состоянии поддерживать нормальное функционирование ткани.
Е. Побел и соавторы приводят целый ряд причин, которые приводят к нарушению процессов посттравматической остеорегенерации:
- Возраст пациента
- Характер травматического повреждения
- Патологическое состояние костной ткани (остеопороз)
- Отягощенный анамнез (хронические болезни печени и почек, ожирение)
- Снижение остеорепаративного потенциала (дефицит факторов роста, остеокальцитонина, активной формы гормона витамина D3)
- Травматичность процедуры металлоостеосинтеза.
Эти изменения приводят к нарушению процессов консолидации костных отломков и требуют проведения мероприятий по оптимизации репаративного остеогенеза.
Кость является высокоспециализированной тканью, которая существует в тесном взаимодействии связи с кровеносной системой. Взаимосвязь путей гемоциркуляции в костной ткани проявляется как в местных нутритивных процессах, поддержке общего минерального равновесия внутренней среды организма, так и непосредственно в физиологической и репаративной регенерации костной ткани.
Поэтому весомым фактором, обусловливающим расстройства репаративного остеогенеза, является нарушение кровообращения в участке повреждения.
Недостаточная степень кровоснабжения зоны перелома вследствие массивного повреждения мягких тканей, кости, отслоение и травматизация надкостницы, нарушение медуллярного кровообращения приводят к активизации хондрогенеза и неполноценности процесса срастания костных отломков.
Проведенные исследования выявили особенности структурно-функционального состояния сосудов при нарушениях репаративного остеогенеза. Эти расстройства могут быть обусловлены структурно-функциональнимы изменениями сосудов поврежденной конечности, которые определяют особенности его течения.
Большой интерес вызывает концептуальная модель механизма компенсации нарушений регионарного кровоснабжения при переломах костей, которую разработали исследователь Г.В. Гайко и его коллеги.
Проводя экспериментальные и клинические исследования периферического кровоснабжения при переломах, авторы пришли к выводу, что в основе восстановления регионарного кровоснабжения после перелома костей лежит перераспределение циркуляции крови и реваскуляризация тканей.
Компенсация регионарного и местного кровоснабжения, как правило, наступает в течение нескольких часов после травмы при переломах без смещения костных отломков, без обширного повреждения мягких тканей и магистральных сосудов.
Неполная компенсация сопровождается гипоксией, способствует развитию фиброзной соединительной ткани и стимулирует фиброзное сращение костных отломков.
На участке декомпенсации возникает некроз костной и мягких тканей, который и является причиной продления сроков лечения, формирования ложных суставов и возникновения гнойных осложнений.
Стадии репаративной регенерации костной ткани
Разработаны стадии репаративного остеогенеза в их взаимосвязи, при которых каждая стадия характеризуется определенным морфологическим клеточно-тканевой составом.
Изучение морфологических изменений при лечении перелома кости с использованием различных методических подходов позволило выделить в регенерации два этапа:
- Построение соединительнотканной мозоли и замещение ее незрелой.
- Перестройка в сформированную зрелой костью предшественницу костной мозоли.
Согласно результатом проведенных патоморфологических анализов заживления костных переломов выделяют следующие стадии восстановления дефекта кости:
- I – дестабилизация клеточных элементов
- II – интенсивная клеточная пролиферация
- III – дифференциация различных тканей (хрящевой, фибробластической, остеобластической, недифференцированной ткани, похожей на мезенхиму, фибробластической соединительной ткани)
- IV – эпигенез остеогенной ткани, при котором наблюдаются процессы прямой метаплазии, атипичной энхондральной оссификации и остеоидной модификации
- V — спонгизация остеоидной ткани и образование остеонов
- VI – образование пластинчатой кости.
В другом варианте выделяются 4 стадии: пролиферацию остеобластных клеток, образование коллагеновых волокон, образование аморфного углеводно-белкового вещества и импрегнация межклеточного вещества минеральными солями.
Используя новые данные молекулярной биологии, биохимии, морфологии, иммуноморфологии и генетики Н. Корж и соавторы выделили 5 стадий репаративного процесса: воспаление, дифференцировку клеток и формирование тканеспецифических структур в области травмы, реорганизация тканевых структур и их минерализация, ремоделирование и завершения восстановительного процесса.
Такого же мнения придерживаются многие известные зарубежные авторы.
Вообще, восстановление кости – сложный биологический процесс, требующий изменений в экспрессии нескольких тысяч генов.
Чаще консолидация переломов происходит путем косвенного восстановления кости, состоит из нескольких последовательных этапов – воспаление, образование мягкой мозоли, образование твердой мозоли и ремоделирование.
Фаза воспаления начинается непосредственно после травмы и длится до 5 дней.
Эта стадия включает образование воспалительной гематомы вследствие разрыва кровеносных капилляров в зоне перелома, миграцию в зону воспаления мезенхимальных клеток, нейтрофилов и макрофагов для удаления фрагментов поврежденной ткани, которые дифференцируются в фибробласты, остеобласты иил хондробласты с последующим образованием хрящевого матрикса.
В течение второй стадии, которая продолжается до 40 дней, происходит замещение гематомы фиброзно-хрящевой тканью путем дифференцирования мезенхимальных клеток в хондроциты, а также синтеза матрикса из коллагена второго типа.
Далее матрикс постепенно кальцинируется и замещается костной тканью, синтезированной остеобластами.
В течение третьей стадии процесса происходит оссификация, образуются костные мостики между фрагментами переломанной кости.
Процесс репаративной регенерации заканчивается стадией ремоделирования, когда восстанавливаются ее исходная форма, структура и механическая прочность.
Нарушение течения любой из этих стадий могут привести к замедлению процесса остеорепарации в целом или даже несращению фрагментов кости.
Гистологически различают два варианта сращения костных отломков – первичное (прямое) и вторичное. Первичное заживление происходит благодаря активной пролиферации остеогенных клеток в фоне гиперваскуляризация тканей на участке перелома. Вторичное заживление протекает в несколько стадий.
На сегодняшний день было разработано несколько классификаций, подробно описывающих стадии заживления перелома.
Известны данные и о стадийности заживления переломов, которые основаны на конкретных морфологических преобразованиях в зоне дефекта кости:
- Тромбирование гематомы
- Организация кровяного сгустка
- Образование фиброзного предкистозного регенерата
- Формирование полноценного регенерата костной ткани
- Образование вторичного регенерата кости
- Функциональная реконструкция регенерата.
Ряд авторов по совокупности структурно-морфологических и биохимических изменений, происходящих в костном регенерате, выделяют следующие фазы регенерации кости:
- I – катаболическая, с дезинтеграцией и деградацией окружающих структур
- II – прогрессирующая пролиферация клеток и дифференцировка клеточных элементов с секрецией органической основы костного регенерата
- III – сложные биохимические, биофизические и физиологические процессы, приводящие к появлению первичной костной структуры
- IV — образование пластинчатой костной структуры, обеспечивающей восстановление формы и функции кости.
При сопоставлении с приведенными выше исследованиями оригинально выглядит вариант классификации стадий заживления перелома кости (воспаление, фагоцитоз, фиброзная мозоль, первичная и вторичная костные мозоли), в котором авторы недостаточно обоснованно отделили фагоцитоз от воспаления.
На основании системных представлений и оценки результатов многочисленных клинических и экспериментальных наблюдений динамики сращения костных отломков А.Т. Бруско и соавторы предложили свою стадийность репаративного остеогенеза. Здесь он рассматривается как однонаправленный процесс, протекающий с закономерной последовательностью морфологических изменений регенерата.
Авторы выделили следующие стадии заживления переломов костей:
- I – репаративная реакция
- II – формирование сращения костных отломков
- III – сращение отломков, при котором возможны варианты: а) первичное костное сращение, b) фиброзно-хрящевое сращение, c) вторичное костное сращение
- IV – функциональная перестройка костной мозоли и консолидированных отломков с формированием органной структуры кости.
Как мы видим, проблема регенерации костной ткани занимает особое место в биологических и медицинских знаниях. На данный момент определены ключевые особенности регенерации костной ткани и достигнуты определенные успехи в выяснении биологических механизмов, лежащих в основе репаративного остеогенеза, сформулированы основные тенденции развития науки.
Примеры работ «До» и «После»
Восстановление всех зубов на верхней и нижней челюсти — базальная имплантация
Случай: частичное отсутствие зубов на верхней и нижней челюсти, осложненное тяжелой формой пародонтита (подвижность зубов).
Комплексная одномоментная имплантация нижней челюсти
Случай: на нижней челюсти имелся расшатавшийся мост из 4 передних зубов, после диагностики было назначено удаление оставшихся зубов и косплексная базальная имплантация.
Восстановление всех зубов методом базальной имплантации (март 2012)
Случай: частичная адентия, оголенные корни собственных зубов, пародонтит, повышенная подвижность зубов, сильная атрофия костной ткани в некоторых местах свыше возможных норм для классической имплантации зубов.
Восстановление передних зубов методом базальной имплантации (апрель 2012)
Случай: частичное отсутствие передних зубов и разрушение опорных зубов под протезом, нарушен рельеф десны и межзубных сосочков.
Источники регенерации
Восстановление целостности кости происходит путем пролиферации клеток остеогенного слоя надкостницы, эндоста, недостаточно дифференцированных плюрипотентных клеток костного мозга, а также вследствие метаплазии гиараосальних тканей.
Современные представления о процессах регенерации костной ткани сочетают концепции неопластической и метапластическая теорий. Преостеогенными клетками считают остеобласты, фибробласты, остеоциты, перициты, гистиоциты, лимфоидные, жировые и эндотелиальные клетки, клетки миелоидного и эритроцитного рядов.
При сращения сломанных костей установлена стадийность репаративного остеогенеза, которая имеет условный характер. Деление на стадии не имеет принципиального значения, поскольку они в динамике перекрываются.
Даже при идеальной репозиции и фиксации отломков дифференцировки различных клеток происходит одновременно, и поэтому стадийность репаративного процесса трудно разграничить. Но для выбора оптимальной тактики лечения больных нужно иметь представление о закономерностях репаративного остеогенеза.
Виды мембран
Мембранная техника, которую использует хирург, нужна для изоляции пространства от фиброзной ткани — создания условий для нормальной регенерации ткани. К мембранам предъявляют несколько требований:
- биологическая совместимость;
- прочность;
- предупреждение миграции клеток эпителия;
- соответствующий период резорбции.
В практике применяют два типа мембран:
- Резорбируемые.
Самостоятельно рассасываются через 6-24 недель после наращивания. Мембраны применяют при небольших дефектах (когда нужно нарастить не больше 2 мм) — они не так хорошо держат форму, как следующий вид. - Нерезорбируемые.
Не рассасываются — их устраняют через несколько месяцев после операции.
Для быстрого срастания искусственного материала с костной тканью челюсти в ряде случаев используют мембраны из плазмы крови пациента.
Показания к костной пластике
Когда врач сообщает о необходимости костной пластики, пациент задается вопросом: зачем это нужно? Причины для проведения наращивания костной ткани челюсти могут быть следующими:
- длительное отсутствие одного или нескольких зубов: при утрате зубных корней костная ткань перестает правильно функционировать в процессе пережевывания пищи, остается без должной нагрузки, поэтому истончается и уменьшается в объемах, т.е. атрофируется,
- травмы челюсти: к ним могут относиться повреждения зубов в результате бытовых случайностей, аварий или занятий опасными видами спорта. А также осложнения после удаления зубов,
- воспаления в полости рта: кисты, гранулемы, пародонтит, которые приводят к рассасыванию костной ткани,
- удаление зуба вместе с корнем – процедура наращивания необходима для того, чтобы сохранить объем кости,
- проведение зубной имплантации: для установки имплантов необходимо, чтобы костной ткани было достаточно – иначе конструкции попросту невозможно будет закрепить. Впрочем, есть импланты, которые крепятся в иных отделах кости – о таких подходах к лечению читайте далее.
Если не прибегнуть к костной пластике вовремя и не восстановить зубы, у пациента могут появиться следующие проблемы:
- ухудшится внешняя эстетика улыбки: соседние зубы начнут менять свое положение и искривляться, между ними появятся щели, нарушится прикус,
- изменится овал лица: появятся морщины, губы западут внутрь рта, нижняя челюсть станет визуально меньше,
- возникнет дискомфорт в общении: испортится дикция и артикуляция,
- нарушится пищеварение: качественное пережевывание продуктов питания станет невозможным.
Как проводится костная пластика и какие материалы используются
Костная пластика зубов или наращивание костной ткани – это хирургическая операция, целью которой является восполнение существующего объема челюстной кости. В первую очередь – костная пластика необходима для имплантации зубов. Перед проведением такой операции требуется тщательная подготовка: осмотр врача, сдача анализов, выявление и исключение острых стадий хронических заболеваний, т.е. противопоказаний к хирургическому вмешательству.
В процессе операции будет выполнена анестезия, надрез надкостных тканей, обеспечивающих доступ к кости, фиксация костного материала, ушивание тканей. После пациенту необходимо настроиться на период восстановления – в среднем он занимает около 2-4 месяцев.
После проведения наращивания кости необходимо время, в течение которого подсаженная кость полностью срастется с существующей, то есть станет с ней единым целым. Только после этого можно приступать непосредственно к установке имплантов. Впрочем, в ряде ситуаций, если исходного объема достаточно для первичного крепления имплантата, то подсадка кости может быть проведена одновременно.
Для замещения утраченной костной ткани используются разные материалы. Это могут быть донорские ткани животного происхождения, полученные путем забора у крупного рогатого скота; человеческие ткани, взятые из подбородочных или челюстных отделов (основной вариант) или выращенные в условиях лаборатории – аллопласты1 или искусственные аналоги кости. Существует несколько методик костной пластики, которые используются в зависимости от показаний и индивидуальных особенностей пациента.
Метод подсадки костных блоков
Применяется в случаях, когда требуется нарастить объем кости не только в высоту, но и в ширину. Блоки крепятся специальными винтами и могут приживаться до полугода, после чего винты удаляются (либо они самостоятельно рассасываются), и проводится имплантация. В данной ситуации применяется собственный донорский материал пациента. Плюс в том, что он не будет отторгнут организмом, это практически исключает риск возникновения осложнений с приживаемостью подсаженных блоков. Однако метод достаточно травматичный, ведь он предполагает заживление двух ран одновременно, одной – в месте извлечения донорского материала, второй – в области наращивания.
Направленная костная регенерация
Во время операции в кость подсаживается синтетический костный аналог. Сверху он покрывается специальными защитными мембранами. Дополнительно может быть применена плазма крови, богатая тромбоцитами, полученная из собственного донорского материала. Она стимулирует рост костной ткани. Процесс срастания искусственной и натуральной кости может занимать от 3 до 6 месяцев. При этом мембрана либо рассасывается, либо удаляется хирургическим путем.
Синус-лифтинг
Процедура помогает увеличить объем кости с помощью изменения положения дна гайморовой пазухи. Она проводится исключительно на верхней челюсти. Если требуется нарастить большой объем, то выполняется открытая операция. Если не хватает нескольких миллиметров кости – закрытая, т.е. одновременно с установкой имплантата. В любом случае технология следующая: через надрез в десне и кости дно пазухи приподнимается специальным инструментом, внутрь закладывается искусственный костный материал. Достоинство способа – эффективное восстановление костной ткани. Недостаток – длительность реабилитации. Также нужно учитывать, что для проведения лечения требуется высокий профессионализм врача. Некачественная операция может привести к развитию воспалений и появлению повреждений слизистой оболочки носовой пазухи, а также проталкиванию имплантата внутрь нее.
Методика
Работа выполнена на 30 крысах-самцах линии Wistar (вес 330 – 360 г, возраст 3,5 мес). Крыс содержали в стандартных условиях по 5 особей в клетке с контролируемыми режимами температуры (24 oC) и освещения (в течение 12 ч) и со свободным доступом к воде и пище. Операцию по моделированию травмы проводили под общим наркозом. Сначала животных анестезировали легким эфирным наркозом. Для более глубокого наркоза, использовали хлоралгидрат, внутрибрюшино, в дозе 300 мг/кг. Затем животное фиксировали на операционном столике, состригали шерсть в области левого бедра и скальпелем разрезали кожу и мышечную ткань. Бедренную кость в области тазобедренного сустава обнажали, просверливали бедренную кость до костномозгового канала на 8-10 мм дистальнее сутава с помощью миниатюрной стоматологической бормашины (диаметр бора 0,8 мм). После повреждения кости производили послойное ушивание мягких тканей. Животных разделяли на две группы. Контрольную (15крыс) и опытную (15 крыс). У подопытных животных с помощью прибора «Остеон-1» проводили стимуляцию области травмы по 5 мин ежедневно в течение 7 сут. (оп7), 14 сут. (оп14) и 21 дня (оп21). Для этого животных фиксировали на операционных столиках и через введенные под кожу хирургические иглы подавали смешанный сигнал из двух импульсных напряжений разной скважности, один из которых модулирован более высокой частотой. Сигналы были не синхронизированными относительно друг друга, однополярными с изменяющимися частотами и амплитудами. Катод располагался в области травмы, анод помещался на ту же лапу дистальнее. Электростимуляцию осуществляли под общим наркозом (хлоралгидрат в дозе 190-200 мг/кг, внутрибрюшинно).
Три группы животных с нанесенной травмой служили контролем (к7, к14, к21), они также располагались на препаровальных столиках, им вводились хирургические иглы, но стимуляция не осуществлялась. В каждом варианте опыта использовали по 5 животных. На следующий день по окончании исследований животные выводились из эксперимента путем цервикальной дислокации. Затем извлекали бедренные кости всех 6-ти групп, которые использовали для гистологического анализа и оценки выраженности патологического процесса и процесса остеогенеза.
Кости животных фиксировали 24 часа при комнатной температуре в 10% формалине, приготовленном на фосфатно-солевом буфере (ФСБ, 0,02М, рН7.6). Декальцинировали в 5% трихлоруксусной кислоте 48 часов, затем промывали в ФСБ и замораживали в изопентане при -400С. Далее приготавливали срезы толщиной 5 мкм. Срезы высушивали при комнатной температуре в течение 1 часа и окрашивали гематоксилин-эозином. Для гистологического анализа от каждого животного было изготовлено от 100 до 200 серийных срезов бедренной кости, сделанных в поперечном и продольном направлениях. С помощью микроскопа Олимпус (ок. 10х, об. 4х). делали микрофотографии срезов костной ткани. Морфометрический анализ костной ткани внутри раневого канала (интермедиарная костная мозоль) осуществляли с помощью программы ImageJ [19]. Площадь костной ткани, измеренной на 3-5 срезах от каждого животного, выражали в % от площади канала. Для определения достоверности различий между опытом и контролем использовали непараметрический двусторонний критерий Манна-Уитни (U-тест).
Что такое направленная костная регенерация
Направленная костная регенерация — это операция по возмещению недостатка костной ткани заменителем, который закрепляют барьерной мембраной. После процедуры вокруг трансплантата образуется каркас (его формируют сосуды и клетки-остеоциты, которые продуцируют новую ткань). Натуральная кость постепенно заменяет искусственный материал.
Наращивание методом НРК производят по классическим параметрам:
- толщина вестибулярной костной стенки (у щеки) — до 2-2,5 мм;
- толщина кости между имплантатом и корнем соседней единицы — до 2,5-3 мм;
- толщина костной стенки между двумя титановыми корнями — до 3 мм.
Можно ли проводить одновременно с имплантацией
Две операции комбинируют в одну при соблюдении условий:
- форма дефекта позволяет правильно установить искусственный корень в любой из плоскостей;
- при установке имплантат находится в пределах костного контура (не выходит за касательную, проведенную к линии кости);
- устраняют горизонтальный (не вертикальный) дефект.
Вживленный имплант может стать барьером для роста кровеносных сосудов и тормозить формирование новой кости. Если имплантат выступает за контур костной ткани, не исключают риск получения сформировавшейся фиброзной ткани с включениями подсаженного материала.
Какие костные материалы применяются
Остеопластика предполагает использование материалов, заменяющих кость. Ранее использовались трансплантаты, которые не получили широкого применения по причине частых отторжений чужеродного материала:
- Аллотрансплантанты
— донорская кость других людей. Материал получали от трупов, обрабатывали, стерилизовали, хранили в банках костной ткани. - Ксенотрансплантаты
— кости животных (крупного рогатого скота, свиней). Материал освобождали от белков методом нагревания (для исключения вероятности аллергической реакции после пересадки).
Мы не применяем устаревшие методики. Сейчас разработано множество синтетических компонентов, способствующих росту собственной кости, которые мы используем для наращивания костной ткани.
Синтетические материалы имеют высокую степень сродства и совместимости с натуральной костью, являются ее аналогами. Это гранулированные составы на базе:
- фосфатов кальция;
- хондроитин-сульфата;
- биостекла.
Эффективность и безопасность искусственных материалов подтверждена многочисленными исследованиями. Они просты в применении, хорошо приживаются, способствуют регенерации собственной кости, гипоаллергенны.
При остеопластике возможна комбинация искусственного заменителя и собственной кости человека в форме стружки (аутотрансплантат). Методика помогает сохранить объем заложенной костной ткани и ускорить темпы восстановления. Этот же метод выручает, если предстоит нарастить большой объем ткани.
При небольшом дефиците можно обойтись только синтетическими материалами.
Преимущества и недостатки костной пластики
В давние времена не существовало профессии «дантист»: если требовалось удалить зуб, люди с опаской шли к дилетантам в области медицины, у которых имелись инструменты, пригодные для таких манипуляций – к парикмахерам и кузнецам. В настоящее время можно решить любые проблемы с зубами безболезненно, эффективно и профессионально, но у многих просыпается «первобытный» страх. Операция по наращиванию костной ткани не является исключением.
Боязнь процедуры может стать серьезным препятствием к восстановлению полноценной улыбки. Если пациент нуждается в костной пластике, важно понимать преимущества, которые дает операция, а именно – восстановление полноценного объема кости. Это дает возможность провести имплантацию, которая в дальнейшем решит более глубокие проблемы, а именно – восстановит эстетику и функциональность зубов. Что касается недостатков – то они связаны с материальными затратами (операция достаточно дорогостоящая), длительностью (процедура откладывает имплантацию минимум на 2-3 мес.), а также сложной реабилитацией. В первые дни после костной пластики могут беспокоить боли, отеки и кровотечения. Симптомы хорошо купируются местными обезболивающими препаратами и антисептиками. Кроме того, существуют ограничения по перелетам, питанию, физическим нагрузкам. Согласно статистике, вероятность серьезных осложнений после операции составляет всего 1-3%, и только при условии, что пациент халатно относится к рекомендациям своего лечащего врача, либо операция была проведена непрофессионально.
При грамотном и профессиональном подходе пациент не узнает, что такое осложнения после костной пластики. Но вопрос в другом – нужно ли проводить данную процедуру, если сегодня существуют методики имплантации, которые со столь же высоким результатом, позволяют обойтись без наращивания кости? Мы успешно применяем методы имплантации зубов с немедленной нагрузкой – в 90% всех случаев пластика кости не требуется