Остеопластика в стоматологии – наращивание костной ткани, необходимой для удачной имплантации. После того, как человеку удалили зуб, твердая ткань имеет свойство рассасываться, а новый искусственный зуб должен надежно держаться в челюсти. Наращивание кости для имплантации зубов успешно решает эту проблему, но требует дополнительных затрат и больше времени (чем, например, при одномоментной имплантации, когда объема ткани достаточно).
Остеопластика – что это такое, и зачем она нужна?
При внедрении титанового корня очень важно, чтобы он со всех сторон был окружен костью. Если есть дефицит ткани, то титановый штифт будет отторгаться. Более того, если корень установлен в верхнюю челюсть, есть риск задевания верхнечелюстных пазух, что может привести к серьезным ЛОР-заболеваниям. Также при недостатке кости имплантат будет расшатываться, опустится ниже десны, что скажется на эстетике протеза и общей картине.
Остеопластика рекомендована в таких случаях:
- если необходимо установить корень в зону, где свой зуб был удален несколько лет (или месяцев) тому назад;
- если у пациента анатомически большие гайморовые пазухи;
- когда физиологически у человека минимальный объем твердой ткани.
Операция не выполняется, если:
- у пациента хронические ЛОР-заболевания (гаймориты, синуситы, риниты);
- нехватка кальция в организме;
- есть патологии в строении дыхательной системы;
- онкология;
- полипы и другие образования в носу;
- сахарный диабет.
Также остеопластика не выполняется беременным и кормящим женщинам. В остальном, операция делается относительно быстро и с гарантией.
Во многих случаях пациентам перед операцией рекомендуют пропить курс гормональных препаратов и антибиотиков, чтобы нейтрализовать отечные состояния и возможные воспаления.
Расщепление альвеолярного отростка –
Используется при горизонтальной резорбции кости для увеличения толщины альвеолярного отростка. Может проводить как на нижней, так и на верхней челюсти. Нужно сказать, что это самый эффективный метод расширения альвеолярного отростка на сегодняшний день, который к тому же имеет малую себестоимость (он не требует дорогих костных материалов и мембран). Существует несколько разновидностей такого расщепления, но особо мы остановимся на методике «Split-Control», которая позволяет одновременно провести и расширение, и установку имплантов.
Содержание методики «Split-Control» (рис.5-10) – после отслойки слизисто-надкостничных лоскутов (десны) по центру гребня альвеолярного отростка делается пропил фрезой или же другими специальными инструментами на высоту будущего импланта (рис.6). Далее пилотным сверлом намечается отверстие под имплант(ы) и в подготовленные отверстия вкручиваются спредеры (рис.7). Использованием разных размеров спредеров от меньшего к большему – можно увеличить ширину гребня и сразу установить имплант.
По бокам импланта всегда остается щель, которая заполняется костным материалом, который при необходимости можно нанести с избытком и снаружи альвеолярного отростка, прикрыв это все специальной резорбируемой мембраной (рис.9). После чего рана ушивается, и мы ждем остеоинтеграции импланта в течение 3-4 месяцев.
Костная пластика нижней челюсти (метод расщепления) –
Плюсы методики –
- Во-первых – благодаря расщеплению гребня мы получаем костный дефект, который имеет костные стенки со всех сторон (кроме как сверху). Благодаря этому происходит быстрый и качественный остеогенез (образование новой кости), ведь губчатая кость в глубине альвеолярного отростка богата кровеносными сосудами, остеобластами, мезенхимальными клетками, факторами роста…
К слову о том, почему гораздо хуже увеличивать ширину кости не за счет расщепления (изнутри альвеолярного отростка), а делать это за счет внешнего прикрепления костных блоков или костной стружки снаружи кортикальной пластики альвеолярного отростка (24stoma.ru). Дело в том, что внешний кортикальный слой кости очень плотный и в нем практически отсутствуют сосуды. Соответственно, подсаживаемый костный материал будет очень долго прорастать сосудами, медленнее будет идти образование кости, будет больше риск неудачи и осложнений такой костной пластики.
- Во-вторых – тут не нужно дорогих костных материалов и мембраны, опять же за счет того, что это трехстеночный дефект внутри альвеолярного отростка, а не снаружи его. Тут достаточно недорогих материалов, например, костного материала «Остеодент-К» и мембраны «Остеодент-Барьер». Но если вы принципиальны, то можно использовать и дорогие материалы типа «Bio-Oss».
- В-третьих – установка имплантов при этой методике в большинстве случаев возможна сразу. Если импланты будут устанавливаться позже, то между операциями должно будет пройти всего 3-4 месяца, что значительно меньше, по сравнению с другими методиками костной пластики.
Расщепление альвеолярного отростка: анимация и видео операции
Важно: существуют несколько разновидностей методики расщепления. При «Split-Control» фрезой делаются только пропил по гребню альвеолярного отростка + пара вертикальных пропилов на толщину кортикальной пластинки. Но существует разновидность этого метода, где делается еще и дополнительный горизонтальный пропил на уровне верхушек будущих имплантов, что приводит к полному отсоединению костного блока (вестибулярной кортикальной пластинки).
Потом этот блок фиксируют винтами, которые его часто и ломают. Импланты при такой модификации методики устанавливают не сразу, а спустя 3-4 месяца. Кроме того, это весьма травматично и больше риск осложнений. Эта разновидность методики должна применяться только при самом тонком альвеолярном отростке (2 мм), но некоторые врачи используют ее даже в тех случаях, когда этого делать не нужно.
Типы костной ткани в стоматологии
- аллотрансплантат – синтетическая костная ткань в стоматологии, которая создается в лабораторных условиях. Это искусственный материал, который не всегда успешно приживается;
- внутриротовой аутотрансплантат – собственная костная ткань пациента, которая была взята из других зон ротовой полости. Например, из самой дальней части зубного ряда. Подобная процедура наращивания называется аутотрансплантацией;
- аллогенный костный материал в хирургической стоматологии – человеческая кость, донором которой является другой пациент. Высокие показатели приживаемости, но пациента может смущать, что этот материал взят из трупной кости, хоть и хранился в стерильной упаковке;
- ксенотрансплантат – заменитель костной ткани в современной стоматологии, материал животного происхождения. Заимствуется из костей крупного рогатого скота. Один из самых востребованных материалов для трансплантации, когда требуется большой объем твердой ткани;
- гранулы гидроксиапатита – искусственный костный трансплантат в стоматологии.
Определить конкретный вид костного материала в стоматологии вам поможет опытный стоматолог-имплантолог, который изучит состояние пациента, особенности ткани и оценит будущий фронт работ по восстановлению зубного ряда.
Репаративная регенерации костной ткани представляет собой восстановление после повреждения. Этот процесс имеет большое значение для практической медицины. Костная ткань уникальна, поскольку кость способна полностью восстанавливать даже значительные дефекты в отличие от всех других тканей, в которых регенерация завершается образованием соединительнотканного рубца или гипертрофией органа.
Единого определения термина «репаративная регенерация» не существует. Одни авторы утверждают, что это разновидность физиологической регенерации, которая происходит в условиях экстремальных воздействий на организм, но отличается большей интенсивностью. Другие характеризуют ее как сложный процесс, который вызван разрушением костных структур, количественно превышающий допустимые пределы физиологической регенерации и направленный на восстановление целостности и обеспечения функции.
Процессы регенерации костной ткани челюстно-лицевой области представляют собой сложное переплетение ряда общих воздействий на системном уровне и локальных изменений тканевого метаболизма, включая изменения на молекулярном уровне. В основе репаративной регенерации лежат дифференцировки клеток, их пролиферация, резорбция поврежденной ткани и новообразования кости в ходе ремоделирования, а также формирования органического внеклеточного матрикса с последующей его минерализацией.
Стадии заживления костной ткани челюстно-лицевой области
При заживлении переломов выделяют следующие четыре стадии: репаративная реакция, формирования сращений костных отломков, сращение костных отломков, функциональная перестройка костной мозоли и отломков с формированием органной структуры.
В настоящее время исследователи выделяют несколько стадий репаративной регенерации:
- Катаболизм тканей, дифференциация и пролиферация клеточных элементов.
- Образование и дифференциация новых тканевых структур.
- Формирование сосудистых образований для питания новой ткани.
- Перестройка первичного регенерата.
В первой стадии, репаративной реакции кости, различают такие фазы, как острое посттравматическое нарушение тканевого кровоснабжения, некроз клеток с дезорганизацией клеточных структур, пролиферацию нежизнеспособных мезенхимальных стволовых клеток и дифференциацию пролиферирующих клеток в направлении образования костного дифферона (мезенхимальная стволовая клетка — преостеобласт — остеобласт — остеоцит).
Острые посттравматические нарушения тканевого кровоснабжения в области перелома сопровождаются разрывом периоста, эндоста, каналов остеонов, а также костного мозга, сосудов и нервов, мышечной и соединительной тканей, окружающих кость. Данные процессы сопровождаются кровоизлияниями, отеком, макрофагальной инфильтрацией и развитием диффузных ишемических дегенеративнонекротичних изменений в тканях. Указанная фаза продолжается порядка 6-18 часов с момента перенесенной травмы.
Вторая фаза, длительностью 10-24 часов после травмы, сопровождается дезорганизацией структур костной ткани, признаками некроза и макрофагальной клеточной инфильтрацией.
В третьей фазе, которая приходится на промежуток 24-72 часа с момента перелома, на фоне восстановленного кровоснабжения наблюдается пролиферация мезенхимальных стволовых клеток, перицитов микроциркуляторного русла, периоста, эндоста с формированием остеогенной ткани. В зависимости от расположения пролиферирующих клеток выделяют периостальные (клетки периоста), эндостальные (клетки костного мозга) и интермедиарные (клетки костного мозга и сосудов центральных каналов) костные образования.
Четвертая фаза репаративной реакции сопровождается пролиферацией и дифференциацией остеогенных клеток в преостеобласты и остеобласты. Они синтезируют остеоид, который после минерализации превращается в грубоволокнистую костную ткань. Наблюдается активация остеокластов, что резорбируют некротизированную костную ткань.
На стадии формирования сращений костных отломков, которая наступает на 3-5 сутки с момента травмы, образуется костный регенерат, или мозоль, который распространяется в проксимальном и дистальном направлениях. Спустя 2-6 недель этот процесс приводит к слиянию и консолидации костных отломков.
Последняя стадия заживления перелома характеризуется образованием костных сращений, которые могут быть нескольких типов. Первичное костное сращение сопровождается прямым сращиванием отломков на уровне кортикального слоя с формированием новых остеонов. Фиброзно-хрящевое сращение характеризуется развитием в зоне перелома некроза костной и мягких тканей, вялой репаративной реакцией, развивающейся на значительном расстоянии от места перелома, и преимущественным развитием фиброзной, реже хрящевой ткани.
Сложившееся фиброзно-хрящевое сращение кости в результате длительной оссификации может замещаться костной тканью, образуя вторичное сращение костных отломков. В четвертой стадии происходит функциональная перестройка костной мозоли и сросшихся отломков с формированием органной структуры кости.
Клетки и вещества, участвующие в репаративной регенерации
костной ткани
Процесс регенерации костной ткани челюстно-лицевой области происходит при участии таких клеток, как остеобласты, остеокласты или остеоциты. Ниже приведена краткая характеристика этих клеточных элементов с указанием особенностей их структуры и функций.
Остеобласты
представляют собой костеобразующие клетки, которые происходят из мезенхимальных стволовых клеток. Они округлой формы, размером 20-30 мкм, с эксцентрично расположенным ядром. Эти клетки располагаются в остеогенном слое надкостницы и в периваскулярных пространствах остеонов.
Выделяют четыре типа остеобластов, участвующих в заживлении костной ткани: преостеобласты, пролиферирующие функционально активные остеобласты, созревающие с гипертрофированной эндоплазматической сетью остеобласты, а также дифференцированные малоактивные остеобласты. Основная часть остеобластов синтезируют костную ткань, пока не наступит остановка их функции с последующим превращением их в неактивные клетки.
Эти клетки выстилают поверхность вновь созданной костной ткани, и при помощи системы канальцев соединяется с остеоцитами. Определенная часть остеобластов инкапсулируется в остеоидный матрикс и дифференцируются в остеоциты.
Остеобласты имеют развитый аппарат Гольджи и митохондрии, благодаря чему синтезируют огромное количество межклеточного вещества, в частности протеины и коллагеновые волокна, которые образуют органический костный матрикс — остеоид. Остеобласты синтезируют коллаген I типа из проколлагена, который состоит из одной α2- и двух α1-полипептидных цепочек, образующих спиральную структуру.
Молекула проколлагена содержит два конечных пептида: амино- и карбокситерминальные пропептиды. После секреции проколлагена остеобластами в экстрацеллюлярное пространство эти два пропептида под влиянием энзимов отщепляются от проколлагена, который трансформирутеся в тропоколлаген.
Свободные конечные пропептиды костной ткани попадают в циркулирующую кровь, где можно определить их концентрацию иммуноферментным методом. Этот анализ очень точно указывает на количество синтезированного коллагена I типа, причем уровень аминотерминального пропептида наиболее точно характеризует его метаболизм.
Также остеобласты синтезируют неколлагеновую фракцию белков костного матрикса, которым принадлежит ведущая роль в его минерализации. Это остеокальцин, остеопонтин, остеонектин, и костный сиалопротеин.
Остеокальцин — основной неколлагеновых белок кости, который участвует в связывании кальция и гидроксиапатитов. Он оказывает хемотаксическое воздействие на остеокласты и принимает участие в резорбции кости.
Остеонектин связывает коллаген I типа и гидроксиапатит, принимает участие в образовании начального кристалла (нуклеации) при минерализации кости. Остеопонтин также связывает костные клетки с гидроксиапатитом внеклеточного пространства, но исследования последних лет указывают на участие этого белка в метастазировании опухолей путем облегчения адгезии опухолевых клеток в процессе инвазии.
Костный сиалопротеин содержит сиаловые кислоты. Он является кальцийсвязывающим гликопротеином, обеспечивающим минерализацию и стабилизации структуры коллагена.
Остеоциты
, или «звездчатые клетки», имеют большое количество длинных и тонких отростков. Они делятся на три типа, характеристики которых кратко перечислены ниже:
- Остеоциты I типа, продуцирующие клетки, синтезируют компоненты костного матрикса.
- Остеоциты II типа, зрелые или резорбирующие клетки, участвуют в процессе остеолиза.
- Остеоциты III типа, дегенерирующие клетки, располагаются на периферии остеона. Вследствие их деструкции высвобождается значительное количество лизосомальных ферментов и происходит остеолизис костной ткани.
Остеоциты имеют рецепторы к паратгормону, синтезируют остеокальцин, матриксные протеины и склеротин, который является ингибитором Wnt-сигнала в остеобластах. Главной их функцией является передача механического и химического сигналинга остеобластам, покровным клеткам и через них — остеокластам. Эта цепочка играет важную роль для запуска процессов ремоделирования кости в физиологических и в патологических условиях.
Остеокласты
представляют собой многоядерные гигантские клетки, которые обеспечивают резорбцию компонентов костного матрикса. Они расположены на поверхности кости в небольших углублениях (эрозионные лакуны или лакуны Хаушипа). В местах контакта с участками резорбции кости цитоплазма остеобластов образует выросты в виде гофрированной каймы, что увеличивает площадь контакта с костью и облегчает поступление в зону резорбции биологически активных клеточных продуктов.
Также остеокласты секретируют в зону резорбции протоны и протеолитические ферменты (катепсин К, цистеинпротеазу, матриксные металлопротеиназы) и удаляют через базолатеральную мембрану продукты распада в окружающее пространство. Для осуществления такого транспорта необходимо присутствие тартратрезистентной кислой фосфатазы (ТРКФ). Существует 5 видов кислых фосфатаз, которые производятся костной тканью, селезенкой, эритроцитами, тромбоцитами и макрофагами. Все виды кислых фосфатаз ингибируются тартратом, кроме пятой изоформы, которая называется ТРКФ-5.
Остеокластогенез,
остеобластогенези ремоделирование кости
Различают следующие функциональные типы остеокластов: молодые, зрелые, функционально активные и неактивные, а также погибающие. Источником происхождения всех остеокластов являются макрофагально-моноцитарные клетки костного мозга.
Важная роль в остеокластогенезе принадлежит системе RANK / RANKL / OPG, которая была открыта в 1997 году. RANKL, экспрессируемый на поверхности остеобластов, связывается с RANK-рецептором, который расположен на мембранах клеток-предшественников остеокластов. Это запускает дифференциацию и активацию остеокластов. Взаимодействие RANKL и RANK происходит в присутствии макрофагального колониестимулирующего фактора (M-CSF), который при помощи высокоафинных трансмембранных рецепторов (c-fms) активирует внутриклеточную тирозинкиназу и стимулирует пролиферацию и дифференциацию предшественников остеокластов, мононуклеаров.
Было доказано, что активность M-CSF значительно повышается при воздействии на остеобласты паратиреоидного гормона, витамина Д3 и фактора некроза опухолей (TNF), однако снижается при воздействии OPG и эстрогенов.
Остеопротегерин синтезируется остеобластами, клетками стромы эндотелия сосудов и В-лимфоцитамы. Это растворимый рецептор-ловушка для RANKL, который препятствует взаимодействию RANKL и RANK, что нарушает остеокластогенез и тормозит резорбцию костной ткани. Вместе с тем, интерлейкины (ИЛ) -1,3,6,11, фактор некроза опухолей-α (ФНО-α), гранулоцитарно- макрофагальный колониестимулирующий фактор (GM-CSF) и простагландины Е2 (PG2) через рецептор ЕР4 способны усиливать продукцию RANKL клетками стромы костного окружения, в частности остеобластами, что стимулирует остеокластогенез.
Обнаружено, что продукцию остеокластов стимулирует паратиреоидный гормон. Он синтезируется паращитовидными железами. Гормон поддерживает гомеостаз кальция путем вымывания из кости во внеклеточную жидкость и усиление реабсорбции в канальцах почек. Этот гормон активирует синтез кислой фосфатазы, лактата и цитрата, и подавляет синтез коллагена и щелочной фосфатазы.
При резком повышении уровня паратгормона в крови наблюдается активация зрелых остеоцитов и резорбция кости (остеоцитарный остеолиз). При длительной гиперсекреции паратгормона усиливается остеокластогенез и снижается активность остеобластов, что также подавляет синтез коллагена. Доказано, что длительное введение малых доз паратгормона вызывает анаболический эффект, а это, наоборот, способствует созреванию хрящевой ткани. Он способствует синтезу в почках 1,25-(ОН)-2D3 под влиянием циклического АМФ из 25-(ОН)-2D3.
В отличие от паратгормона, кальцитонин, который секретируется в межфолликулярных клетках щитовидной железы, уменьшает количество и активность остеокластов в костной ткани, подавляет остеоцитарный остеолиз и уменьшает уровень кальция в крови. Кальцитонин стимулирует созревание хондроцитов в эпифизарном хряще.
Согласно зарубежным исследованиям последних лет, ведущая роль в регуляции остеобластогенеза принадлежит костным морфогенетических белкам (BMP, bone morphogenetic protein). Это группа сигнальных факторов роста (цитокины), которыеактивно стимулируют формирование энхондральной костной ткани и регулируют различные клеточные процессы (пролиферацию, дифференцировку, апоптоз, хемотаксис, ангиогенез или продукцию внеклеточного матрикса в тканях).
BMP запускают процесс образования костной ткани за счет экспрессии генов, регулирующих процессы дифференциации мезенхимальных стволовых клеток с последующим образованием клеток-остеобластов. Нарушение регуляции сигнальной системы BMP очень часто обнаруживаются при онкологических заболеваниях.
В настоящее время были описаны 47 белков подсемейства BMP, взаимодействующих со специфическими BMP-рецепторами (BMPs). В процессе межклеточных взаимодействий в костной ткани челюстно-лицевой области особенно важны следующие:
- BMP2: стимулируют дифференцировку остеобластов.
- BMP3: способствуют образованию новой костной ткани.
- BMP7: активируют дифференцировку остеобластов и продукцию SMAD1.
- BMP8a: принимают непосредственное участие в развитии кости и хряща.
В практической медицине BMP используют для стимуляции процессов заживления кости. Их вводят в костный имплантат, откуда они попадают в места перелома для улучшения остеогенеза.
Костные клетки интенсивно выделяют в межкостный матрикс трансформирующий фактор роста β1 (ТGFβ1), который активирует дифференциацию мезенхимальных стволовых клеток по остеобластическому и хондральному типу, стимулируют процессы репаративной регенерации костей, усиливают пролиферацию и синтез коллагена.
Процессы, связанные с морфогенезом клеток, регулирует также Wnt-сингалинг. Этот процесс включает белки, открытые в начале 1980-х годов как маркеры некоторых видов онкологических заболеваний. Они являются также ключевыми регуляторами процессов ремоделирования и регенерации костной ткани, дифференцировки мезенхимальных стволовых клеток.
В основе канонического пути Wnt-сигналинга в костной ткани лежит стабилизация белка цитоплазмы β-катенина. При отсутствии сигнала он неактивен и быстро разрушается. При активации β-катенина через Wnt, сам Wnt связывается с поверхностными рецепторами клеток, в качестве которых выступает трансмембранный белок Фрайзленда. В результате этого тормозится разрушения β-катенина, он накапливается в цитоплазме и после проникает в ядро. Там он взаимодействует с белками TCF / LEF, которые избирательно связываются с определенными белками-активаторами и последовательностями ДНК.
Таким путем происходит активация определенных генов, отвечающих за регенерацию костной ткани. Другой, или неканонический (β-катениннезависимый) путь Wnt-сигналинга регулирует полярность клеток, стимулирует метаболизм кальция и реорганизацию цитоскелета. Передача Wnt-сигналов стимулирует продукцию OPG. Доказано, что у человека в активации Wnt-сигналинга привлечено как минимум 22 Wnt-лигандов.
Антагонистом Wnt / β-катенинсигнального пути является склеротингликопротеид, который производится остеоцитами неповрежденной кости. Он препятствует дифференцировке MSC. При возникновении повреждений костной ткани челюстно-лицевой области остеоциты передают сигнал покровным клеткам, которые выстилают поверхность трабекулы. Под влиянием простагландинов и факторов роста, которые при этом выделяются, покровные клетки отслаиваются от поверхности кости, образуя специфический навес. Клетки навеса сочетаются с остеоцитами, с капилляром и образуют компартмент костного ремоделирования.
Недавно были открыты такие регуляторы межклеточных взаимодействий между остеобластами и остеокластами, как семафорины и их рецепторы плексины. Cемафорины образуют семейство молекул из 8 основных классов секреторных и трансмембранных белков, которые отвечают за передачу сигналов по аксонам. Они регулируют рост, развитие и функционирование клеток нервной, сердечно-сосудистой, иммунной, дыхательной, а также опорно-двигательной систем.
В частности, Semaphorin 4D (Sema4D), который является производным остеокластов, действует на мембранный рецептор Plexin-B1 на поверхности остеобластов, подавляя функцию последних. В результате наблюдается активация резорбции костной ткани. Семафорин 3В способствует активации остеокластов, а семафорин 3А, наоборот, стимулирует остеогенез. Исходя из этого, для лечения остеопении важное значение имеет ингибирование семафоринов 4D и 3В.
Важным секреторным производным остеокластов является белок SLIT3. Он стимулирует пролиферацию клеток-остеобластов благодаря активации β-катенинового пути. Аутокринная сигнализация SLIT3 ингибирует резорбцию костной ткани путем подавления дифференцировки преостеокластов. В экспериментальных исследованиях было показано, что модифицированные животные с отсутствием SLIT3 или его рецептора Robo 1 имеют низкие показатели образования костной ткани и высокую скорость ее резорбции.
Практическая оценка процессов регенерации костной ткани
Процессы ремоделирования костной ткани можно наглядно оценить на основании сравнительного анализа двух групп показателей костного метаболизма — маркеров костной резорбции (гидроксипролин, оксипролин, кальций, продукты распада коллагена I типа, пиридинолин и дезоксипиридинолин , костный сиалопротеин (BSP), тартратрезистентна кислая фосфатаза) и маркеров синтеза кости (остеокальцин, костная щелочная фосфатаза, амино и карбокситерминальные фрагменты проколлагена I типа, АКФ, ККФ).
Маркеры синтеза костной ткани косвенно характеризует активность остеобластов. Эти клетки принимают активное участие в формировании костной ткани, производят коллаген I типа плюс другие компоненты остеоида, участвуют в минерализации остеоида гидроксиапатитом.
Первым биохимическим маркером костного ремоделирования является фермент щелочная фосфатаза, который в 1929 году был введен в клиническую практику и сегодня применяется. Существует 4 изоформы этого фермента: костная, печеночная, кишечная и плацентарная.
Лабораторным показателем активности остеобластов является костная щелочная фосфатаза. Это гликопротеин, который принимает участие в минерализации костного матрикса. Одновременное повышение КЩФ и паратгормона может указывать на развитие остеодистрофии с высоким уровнем костного ремоделирования, а снижение этих показателей может свидетельствовать об адинамическом состоянии костной ткани челюстно-лицевой области.
Наиболее информативным маркером формирования кости является остеокальцин. Этот неколлагеновый белок костного матрикса, содержащий гидроксиапатит, может считаться специфическим для костной ткани и дентина. Он синтезируется преимущественно остеобластами и формирует внеклеточный матрикс кости.
Фракция вновь синтезированных остеокластов высвобождается в кровоток, поэтому именно этот маркер указывает на скорость ремоделирования костной ткани. Повышенный уровень паратгормона в крови подавляет активность остеобластов, продуцирующих остеокластов, и снижает концентрацию остеокластов в крови и костной ткани.
В процессе синтеза коллагена I типа остеобластами с проколлагена I типа от него в результате действия специфических ферментов отделяются амино- и карбокситерминальные фрагменты. Соотношение между количеством зрелого коллагена, откладывающегося в костный матрикс, и количеством терминальных молекул, которые поступают в кровеносное русло, должно быть равно единице. Благодаря этому по показателям АКФ, ККФ в сыворотке крови можно судить о синтетической активности остеобластов по синтезу коллагена I типа.
Следующая группа показателей костного ремоделирования — это маркеры резорбции костной ткани. Следует отметить, что они в течение суток меняют свой уровень, поэтому определять их необходимо в одно и то же время суток, лучше утром. К маркерам резорбции костной ткани относятся ферменты, участвующие в разрушении костного матрикса под влиянием остеобластов, и продукты разрушения коллагена I типа.
Это, например, тартратрезистентная кислая фосфатаза (TRAP) — металлосодержащий энзим, один из 6 изоферментов кислой фосфатазы. Он секретируется остеобластами в внеклеточную среду во время резорбции. Существуют формы TRAP-5а и 5в, но TRAP-5в синтезируется остеобластами, а TRAP-5а имеет макрофагальное происхождение. Активность TRAP-5в в плазме крови является показателем процессов резорбции кости.
Гидроксипролин является основной аминокислотой в составе коллагена. Он не считается аутоспецифичным маркером костной ткани, ведь только 50% этой аминокислоты находится в костях, а остальные 50% являются компонентом других белков, в частности эластина, ацетилхолинэстеразы и фактора комплемента С1q.
Большая часть его после разрушения коллагена окисляется в печени и только 15% выводится с мочой. Содержание гидроксипролина зависит от характера питания, возраста человека, наличия опухоли с распадом и демонстрирует циркадный ритм с пиком между 0.00 и 8.00 утра.
14% аминокислотного состава коллагена составляет оксипролин. Он синтезируется остеобластами и также является маркером костной резорбции. В наше время используют более специфические маркеры костной резорбции, такие как продукты распада коллагена I типа. К ним относятся пиридинолин (ПИД) и дезоксипиридинолин (ДПИД). Они находятся в тканях, содержащих коллаген I, II, III типа. ПИД является важным химическим соединением, но ДПИД встречается только в коллагене, поэтому его оценивают как селективный костный маркер.
Также широко применяют в медицинской практике определение показателей пептидов коллагена I типа, NTX и СTX. Уникальность этих показателей заключается в быстром росте их уровня при заболеваниях, сопровождающихся высокой резорбцией костной ткани (например, при остеопорозе, метастазах в кости), а также быстрому их снижению (в течение нескольких недель) на фоне антирезорбтивной терапии.
Следующий маркер резорбции костной ткани — это костный сиалопротеин (BSP). В процессе остеолиза (физиологического или патологического) происходит разрушение костного матрикса ферментами остеобластов с выделением в кровь сиалопротеина с соответствующим ростом лабораторных показателей BSP. Костный сиалопротеин присутствует только в зрелых остеобластах и не обнаруживается в их предшественниках, поэтому BSP может служить маркером поздней дифференцировки клеток кости.
Заключение
Репаративная регенерация костной ткани челюстно-лицевой области связана с деятельностью остеогенных клеток. В основе локальной регуляции репаративной регенерации лежат несколько сигнальных путей, такие как молекулярная система RANK / RANKL / OPG, костные морфогенетические белки, Wnt-сигналинг и другие.
Остеобластогенез и остеокластогенез характеризует биохимические маркеры костного ремоделирования, определение которых позволяет установить скорость обменных процессов в костной ткани, выявлять пациентов с повышенным риском и проводить раннюю оценку эффективности назначенного лечения, прогнозировать риск возникновения осложнений, диагностировать на ранних сроках появление костных метастазов и др.
Плюсы и минусы костной пластики при имплантации
Конкурентные преимущества костной пластики:
- восстановление функций, даже если у пациента утрачен большое количество твердой ткани;
- нормализуется внешний вид десневой ткани и ротовой полости в целом;
- восстановление жевательных функций – все виды костной ткани в стоматологии адаптированы под большие нагрузки;
- возможность восстановить зубной ряд, даже в самых запущенных ситуациях.
Недостатки костной пластики:
- реабилитация занимает несколько месяцев;
- высок риск отторжения блока;
- болевые ощущения в процессе приживления тканей;
- немалая цена операции.
Человеческий эмбрион и сперматозоиды
Это похоже на войну миров, на самом же деле перед вами яйцеклетка через 5 дней после оплодотворения. Некоторые сперматозоиды все еще удерживаются на ее поверхности. Изображение сделано с помощью конфокального (софокусного) микроскопа. Яйцеклетка и ядра сперматозоидов окрашены в пурпурный цвет, тогда как жгутики сперматозоидов — в зеленый. Голубые участки — это нексусы, межклеточные щелевые контакты, осуществляющие связь между клетками.
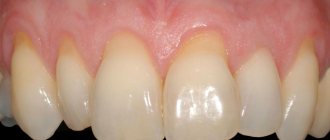
Последствия атрофии
Данное заболевание может привести к определенным последствиям. Главное – это то, что станет невозможным закрепление имплантата и восстановление потерянных зубов. Кроме того, пациент может наблюдать и негативные перемены атрофии кости внешне, то есть меняется форма и вид лица, происходит нарушение функционирования многих органов.
Также атрофия костной ткани зубов может привести к:
- образованию мимических морщинок в зоне губ;
- необходимости проведения дополнительных манипуляций по увеличению костного объема перед тем, как провести имплантацию;
- невозможности пережевывания пищи, соответственно, это приводит к проблемам с желудочно-кишечным трактом;
- «западанию» внутрь губ;
- смещению в сторону зубов, в то место, где есть их отсутствие.
Кроме того, одним из важных последствий этого заболевания считают увеличение цены имплантации. Это объясняется тем, что для закрепления имплантатов потребуется определенный объем кости. Если его будет недостаточно, то нужно будет сделать его наращивание. А это подразумевает использование дополнительных материалов и лекарственных средств, работы специалиста.