4156
До сих пор считается, что лучшими имплантами при операциях на костях является аутогенная (взятая у самого больного) кость. Однако, ввиду ограниченности и выраженной резорбции этот материал, все же, нельзя считать идеальным.
Хорошей альтернативой ему являются костные заменители, получаемые из костей животных. Производимый компанией Geistlich Pharma биоматериал Bio Oss, предназначенный для использования в стоматологии, вмещает в себя все основные достоинства костных заменителей.
Общее представление
Bio Oss получают из костей КРС. Материал имеет несколько лекарственных форм, позволяющих выбрать оптимальный способ подачи в операционную рану:
- Гранулы, расфасованные во флаконы (Bio-Oss Spongiosa). Универсальная форма, подходящая для любого вида операций.
- Гранулы в шприце (Bio-Oss Pen). Благодаря наконечнику особой формы Bio-Oss Pen, особенно удобен в случаях, когда операционная зона находится в труднодоступном месте.
- Блоки (Bio-Oss Block). Применяются, когда требуется заполнение значительных дефектов.
- Комбинированный препарат Bio-Oss Collagen, на 90% состоящий из гранул Bio-Oss, на 10% – из свиного коллагена. Благодаря последнему, обладает повышенными адгезионными, манипуляционными и регенерационными качествами.
Geistlich Pharma выпускает также мембрану Geistlich Bio-Gide – вспомогательный материал, используемый для создания барьера между костью и пазухой. Применение Bio-Gide ускоряет регенерацию тканей и заживление ран.
Geistlich Bio-Oss рекомендуется к применению при любых видах костной пластики – в хирургической стоматологии, имплантологии, пародонтологии, челюстно-лицевой хирургии.
По своим регенерирующим и заживляющим свойством он не только сопоставим с аутогенными костными трансплантатами, но в отдельных компонентах превосходит их.
Кроме того:
- Bio-Oss может использоваться как в одиночку, так и в комбинации с аутогенной костью.
- Костный заменитель эффективно стабилизирует кровяной сгусток, предотвращая луночковое кровотечение.
- Высокая гидрофильность, обуславливаемая наличием множества микро- и макропор, способствует равномерному и быстрому пропитыванию материала физраствором и кровью пациента.
- Стабильность, сохранение объема образующейся костной ткани является выигрышным моментом с точки зрения обеспечения эстетики тканей лица.
- Множественность форм и хорошие манипуляционные характеристики делают возможным использование Bio-Oss в самых разных клинических случаях, в том числе и сложных.
Техника применения Bio-Oss зависит от клинической ситуации и используемой лекарственной формы. Общими являются следующие моменты:
- Пропитывание материала физраствором или кровью пациента.
- Подача его в зону операции и распределение по дефекту.
- Закрытие операционной раны лоскутом мягкой ткани пациента с последующим ушиванием и/или наложение мембраны Bio-Gide.
Выясним вместе, сколько держится температура после имплантации зубов, и в каких случаях необходима помощь специалистов.
Заходите сюда, если интересуют плюсы имплантации зубов.
По этому адресу https://www.vash-dentist.ru/implantatsiya/metodiki/o-prieme-antibiotikov-posle-zubov.html мы расскажем, зачем назначаются антибиотики после имплантации зубов.
Основные преимущества
Костный материал bio oss успешно применяют ведущие врачи-стоматологи уже долгие годы, в частности, специалисты клиники «А-Медик». К его достоинствам относятся:
- стабилизация кровяного сгустка;
- медленная резорбция гранул (она дает возможность сохранить объем аугментата на протяжении длительного периода времени);
- высокая гидрофильность. Она обеспечивается за счет уникальной системе макро и микро пор, гарантирующих равномерное пропитывание гранул кровью;
- остеокондуктивные свойства. Они являются гарантией надежной регенерации. Гранулы интегрируются в образованную кость, становятся ее каркасом;
- гарантия эстетики мягких тканей. Это связано с образованием качественной основы твердой ткани.
Показания и противопоказания
В ортопедии Bio Oss рекомендуется к использованию во всех случаях, когда требуется сохранить или нарастить объем кости альвеолярного отростка или челюсти:
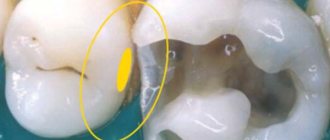
- Заполнение лунки после экстракции зуба для сохранения нормального объема костной ткани, если в дальнейшем планируется имплантация.
- Аугментация (наращивание) кости, производимая одновременно с имплантацией зуба для заполнения зазоров между костью и имплантом.
- Заполнение фенестраций и дегисценций (расхождений и отверстий) в кости после установки имплантов.
- Синус-лифтинг.
- Заполнение полостей в костной ткани челюсти или альвеолы, образовавшихся в результате цистэктомии.
Благодаря сродству Bio Oss с костной тканью человека, биоматериал практически не имеет противопоказаний. Единственное ограничение – его нельзя использовать для заполнения инфицированных ран.
Почему для немедленной имплантации нужны биоматериалы?
Если речь идет исключительно об удалении зуба и установке импланта, то, признаюсь честно, чаще всего они не нужны. Особенно, если учесть, какие зубы чаще всего приходится немедленно имплантировать:
На картинке видно, что немедленная имплантация в эстетически значимой зоне проводится не так часто, как может показаться на первый взгляд. Просто ее проще отснять – именно поэтому все профильные сайты забиты работами в области фронтальной группы зубов, но очень мало случаев немедленной имплантации в боковом отделе зубного ряда.
Тем не менее, немедленная имплантация в боковом отделе зубного ряда проводится гораздо чаще, чем в эстетически значимой зоне. И, чаще всего, использовать какие-то материалы для аугментации лунки при установке импланта не требуется – в большинстве случаев, особенности строения и кровоснабжения альвеолярной кости в этих участках позволяют избежать значительной атрофии.
На приведенных фотографиях заметно, как изменились линейные размеры альвеолярного гребня с момента удаления 26 и установки импланта, до его интеграции (сравните толщину). Но это не так критично, и позволяет получить хороший результат протезирования:
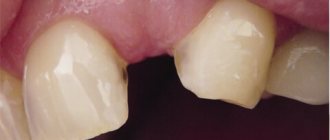
Однако, если одной из задач имплантологического лечения является максимальное сохранение окружающих зуб тканей, то без использования биоматериалов вряд удастся обойтись. На фотографии ниже: вроде как, проведена немедленная имплантация, но последующая атрофия альвеолярного гребня вконец испортила эстетический результат лечения.
Не только фронтальная группа зубов требует внимания с точки зрения эстетики – некоторые пациенты хотят, чтобы и в боковом участке “зуб был неотличим от настоящего”. И в этих случаях мы также используем биоматериалы, чтобы сохранить на месте костные стенки лунки и получить хороший эстетический и функциональный результат:
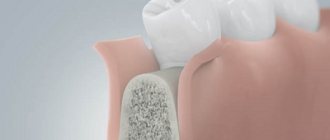
Учитывая то, что имплантат (за редким исключением) всегда меньше, чем удаленный зуб, нам необходимо чем-то заполнить освободившееся от зуба пространство, чтобы удержать окружающие лунку ткани на месте. В противном случае, последующая атрофия может свести на нет эстетические результаты имплантологического лечения:
Согласитесь, не очень приятно, когда имплантат начинает просвечивать… и никакой, даже самой крутой коронкой это не компенсировать.
Так вот, чтобы такого не происходило – нам нужны биоматериалы и графты, в частности. Заполняя пространство между имплантом и стенкой альвеолы, мы удерживаем последнюю на своем месте, предотвращая изменение линейных размеров альвеолярного гребня в области импланта. Безусловно, какая-то степень атрофии все равно присутствует, но она значительно менее выражена и почти незаметна, чем в тех случаях, если бы мы ничего не делали.
Физико-химические характеристики
Кости животных состоят на 25% из органической составляющей (коллагена), на 65% – из неорганики (фосфат кальция) и на 10 % – из воды.
В малых количествах присутствует отличная от коллагена органика – липиды, полисахариды, белки. Кроме кальциевых, имеются ионы некоторых других элементов.
При производстве Био-Осс из сырья (костей КРС) удаляется органическая составляющая. Остается только минеральная основа (фосфат кальция), обильно пронизанная микрокапиллярами и микротоннелями.
По своей морфологии, химическому составу и ультраструктуре Био-Осс очень близок к человеческой кости, что и определяет положительную реакцию на него организма пациента. По сравнению с другими естественными материалами, имеющими более крупные кристаллы, Био-Осс очень хорошо интегрируется с нативной костью.
Важное значение для имплантируемых биоматериалов имеет топография их поверхности. Гладкие материалы интегрируются хуже, чем шероховатые. Био-Осс обладает выраженной шероховатой поверхностью, которая способствует активной адгезии и пролиферации остеобластов, быстрому синтезу матрикса.
Не менее важна и площадь внутренних поверхностей имплантационного материала. Чем она больше, тем интенсивнее врастают в него кровеносные сосуды, активнее и быстрее проходит интеграция и заживление ран. Гистоморфометрические исследования, проведенные с 12-ю образцами костных материалов, показали, что внутренняя поверхность Geistlich Био-Осс составляет около 80 м2/г, что примерно в 5 раз больше, чем у остальных исследованных образцов.
Безопасность
Биоматериал, получаемый из костей КРС, может содержать прионы – особые инфекционные агенты, способные вызывать у животных и человека опасные заболевания. У первых – «коровье бешенство» (ТГЭ, губчатая энцефалопатия).
Люди подвергаются опасности заболевания синдромом Крейтцфельдта – Якоба, куру и некоторыми другими видами инфекций.
Безопасность биоматериала Bio Oss обеспечивается двумя факторами – высоким качеством сырья и технологией обработки, предусматривающей многостадийную очистку и стерилизацию.
При выборе сырья учитывается страна происхождения в части эффективности ветеринарного контроля и мер предосторожностей, предпринимаемых против «коровьего бешенства».
Костное сырье для Био-Осс компания Geistlich Pharma приобретает в США, где ветеринарный контроль действует очень эффективно. До сих пор не было зафиксировано ни одного случая губчатой энцефалопатии.
Для дополнительной гарантии безопасности сырье получают только с 3-х боен, находящихся под постоянным наблюдением USDA.
Вторым фактором, обеспечивающим безопасности материала, является многостадийная очистка сырья, направленная на инактивацию прионов. Кости подвергают температурному воздействию в течение не менее 15 часов.
Дополнительно проводится химическая очистка сырья щелочными соединениями и обработка гамма-облучением. Такая технология гарантирует полную безопасность биоматериала.
Результаты
Недавно мой коллега Андрей Карнеев опубликовал в Facebook фотографию одной работы на финишных этапах протезирования:
Я горжусь тем, что тоже в ней поучаствовал.
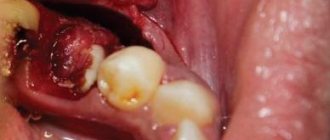
Все началось с воспаления, свищевого хода и удаления зуба:
Затем, мы готовим лунку и проверяем позиционирование импланта:
После чего аугментируем лунку. Для упаковки Bio-Oss Collagen очень удобно использовать аналоги имплантов:
Устанавливаем имплантат XiVE (Dentsply Implants):
Сразу на имплантат – временная коронка:
которая через три месяца, к моменту интеграции импланта, выглядит совсем иначе:
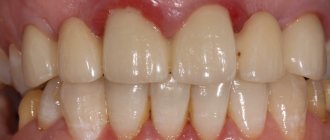
Ну и… к моменту установки постоянной коронки, у нас сохранился естественный контур прилегающей десны.
Что, собственно, нам и требовалось сделать.
Биологические свойства
Остеопластические материалы подразделяются на три группы:
- остеоиндуктивные, непосредственно влияющие на формирование и рост костной ткани;
- остеокондуктивные – исполняют роль каркаса кости, на котором происходит образование новой костной ткани;
- остеонейтральные, выполняющие функцию наполнителя костей.
Bio Oss относится к остеокондуктивным биоматериалам, т. е. выполняет функцию каркаса, на котором образуется и дифференцируется новая костная ткань.
Высокие остеокондуктивные свойства материала обуславливаются большой площадью внутренней поверхности, высокой абсорбцией протеинов и активностью гетеродимерных белков (интегринов), обеспечивающих адгезию клеток к матриксу.
Для микроструктуры характерно наличие большого свободного внутреннего пространства. Это делает материал оптимальным каркасом для вновь образующейся костной ткани.
После операции происходит быстрое и глубокое прорастание кровеносных сосудов в имплантированный материал, активизируется трофик, из тканей пациента в зону дефекта активно мигрируют остеобласты – молодые клетки костной ткани, участвующие в синтезе матрикса. Далее в процессе регенерации остеобласты трансформируются в остеоциты – зрелые ткани кости.
На какие сутки снимаются швы после имплантации зубов и причины их расхождения.
В этой статье подробная информация об имплантации передних зубов.
Здесь https://www.vash-dentist.ru/implantatsiya/metodiki/o-sdache-analizov-pered-zubov.html читайте, какие анализы нужно сдать перед имплантацией зубов.
Коллагеновая мембрана Bio-Gide
Bio-Gide – эталон коллагеновой мембраны для восстановления мягких тканей и кости после хирургических стоматологических вмешательств. Это натуральный продукт высокой степени очистки, который содержит свиной коллаген. Мягкие ткани содержат большое количество коллагеновых волокон, поэтому коллагеновая мембрана используется при восстановлении костной и пародонтальной ткани. Использование Bio-Gide помогает хирургу добиться наилучших и прогнозируемых результатов, дает превосходное заживление раны. Bio-Gide обладает высокой терапевтической безопасностью, которая высоко ценится всеми ведущими хирургами.
Превосходные качества Bio-Gide достигнуты благодаря трехмерной, естественной матричной структуре и высокой биосовместимости. По строению мембрана Bio-Gide очень похожа на человеческий коллаген. На фотографии сверху показан человеческий коллаген под микроскопом, а ниже — мембрана Bio-Gide. Естественная структура коллагена помогает в процессе заживления – кровеносные сосуды прорастают сквозь волокна коллагена.
Мембрана выполняет несколько важных функций в процессе регенерации: защитную, стабилизационную, является основой для мягких тканей.
Мембрана Bio-Gide имеет двухслойную структуру, одна сторона гладкая, а другая шероховатая. Гладкий верхний слой является направляющей для заживления мягких тканей, которое происходит легче, с лучшим эстетическим результатом. Шероховатая сторона мембраны Bio-Gide помогает растущим костным клеткам.
Удалять мембрану не нужно. Распад мембраны на естественные аминокислоты происходит без побочных эффектов, без раздражения тканей.
Ожидаемый эффект применения
Высокая интеграция Био-Осс с нативными костными тканями была установлена множеством гистологических исследований. Отмечалось, что уже через 15 дней после операции остеобласты образовывали на Bio-Oss зрелые коллагеновые волокна.
Около 6-ти недель потребовалось на формирование протяженной сети матрикса – коллагеновых волокон, вплетенных в каркас биоматериала. На гистологических срезах обнаруживались органические вещества, регенерировавшие самостоятельно внутри имплантационной ткани или попавшие туда из крови пациента.
Благодаря медленной резорбции Bio-Oss служит стабильным каркасом для регенерирующей ткани, замедляет рассасывание трансплантата. При исследованиях было установлено, что имплантационный материал из смеси заменителя и нативной кости оказывается стабильней имплантов, в которых аутогенная костная стружка используется в качестве единственного компонента.
В случае применения Био-Осс во время всего наблюдения отмечалось постоянство объема кости, в то время как применение одного аутогенного материала сопровождалось снижением объема имплантационного материала.
Гистоморфометрический анализ подвергнутых восстановлению с помощью Био-Осс тканей показал, что в регенерированной кости объем минеральной составляющей выше, чем в нативной костной ткани.
Это может служить объяснением высокой стабильности имплантов, содержащих Био-Осс в комбинации с аутогенной костью.
Исследовалась также прочность адгезии имплантов в пазухах после синус-лифтинга. Было установлено, что через 3 месяца после операции материалы с Био-Осс имели прочность фиксации на 45% больше, чем импланты из аутогенной кости.
В видео представлена инструкция по применению материала.
При выраженной атрофии альвеолярного отростка в области дна верхнечелюстной пазухи, когда высота костной ткани составляет менее 4 мм, как правило, требуется проведение синус-лифтинга (СЛ) [3]. Для увеличения высоты костной ткани в области дна верхнечелюстной пазухи используется большое количество материалов. Аутотрансплантаты обладают более выраженным регенерационным потенциалом, чем любые другие имплантационные материалы [7, 9]. Однако необходимость забора значительного количества костной ткани, наличие дополнительного операционного поля существенно ограничивают применение аутотрансплантатов [5]. В связи с этим для поднятия дна верхнечелюстной пазухи часто используются имплантационные остеопластические материалы. Имплантационный материал должен быть нетоксичным, обладать остеокондуктивными и остеоиндуктивными свойствами, резорбироваться, не вызывать иммунных реакций. Цель направленной костной инженерии заключается в регенерации кости, которая морфологически и функционально идентична нативной костной ткани [2]. В мировой практике получены положительные результаты восстановления костной ткани в области дна верхнечелюстной пазухи с использованием клеточных трансплантатов [14].
Цель данного исследования — сравнительная оценка эффективности образования костной ткани при использовании двух материалов, применяемых при проведении СЛ: имплантационного материала «Bio-Oss» и тканеинженерной конструкции (ТИК) на основе мультипотентных стромальных клеток (МСК) жировой ткани (ЖТ), преддифференцированных в остеогенном направлении. Клиническое исследование проводили на базе ФГУ «ЦНИИС» Росмедтехнологий совместно с ЗАО «РеМеТэкс».
Материал и методы
Характеристика пациентов.
Клинические наблюдения основаны на обследовании и лечении 25 пациентов с вторичной адентией и выраженным дефицитом костной ткани в области верхней челюсти. Высота альвеолярного отростка до дна верхнечелюстной пазухи, по данным компьютерной томографии (КТ), составляла от 0,9 до 4,8 мм, возраст пациентов — 29—60 лет. Все пациенты были соматически здоровы, всем проведен открытый СЛ: 14 пациентам высота альвеолярного отростка увеличена с помощью ТИК МСК ЖТ, преддифференцированных в остеогенном направлении (группа наблюдения) —
рис. 1
Рисунок 1. КТ до трансплантации ТИК и через 4 мес. — и 11 — путем введения на дно пазухи имплантационного материала «Bio-Oss» (группа сравнения) —
рис. 2.
Рисунок 2. КТ до имплантации ТИК и через 6 мес.
Пациентам с трансплантацией ТИК ЖТ внутрикостная имплантация была проведена через 4 мес после увеличения высоты альвеолярного отростка, а тем, кому имплантировали «Bio-Oss», — через 6 мес. Сроки внутрикостной имплантации были обоснованы ранее проведенным экспериментальным исследованием, в котором изучались сроки и этапы регенерации костной ткани при использовании ТИК ЖТ и «Bio-Oss» [1]. При формировании ложа для имплантатов вместо пилотного сверла использовался трепан диаметром 2 мм для получения биоптатов в виде столбиков.
Для создания ТИК применяли культуру МСК стромально-васкулярной фракции (СВФ) ЖТ. СВФ ЖТ выделяли из липоаспирата. Липоаспирацию выполняли по стандартной методике под местной инфильтрационной анестезией в области передней брюшной стенки. Липоаспират промывали раствором Версена и дезагрегировали путем инкубации в растворе Версена с добавлением 0,25% трипсина при 37 °С в течение 1,5 ч. Клеточную суспензию центрифугировали 10 мин при 1100 об/мин, осадок разводили ростовой средой (DMEM/F12 1:1 с добавлением аутологичной сыворотки до 10%, амикацина до 500 мг/л), переносили в чашки Петри и инкубировали при стандартных культуральных условиях (37 °С, 5% СО2). Ростовую среду меняли каждые 3 сут. Для направленной остеогенной дифференцировки клетки рассаживали на 90 мм чашки Петри и по достижении 80% конфлюентного монослоя заменяли ростовую среду на дифференцировочную (DMEM с 10% аутологичной сыворотки крови, 100 мкг/мл амикацина, 50 мг/л L-аскорбиновой кислоты, 10 ммоль/л β-глицерофосфата натрия и 10 нм 1,25-дигидроксивитамина D3). Замену среды на свежую производили каждые 3 сут.
Приготовление плазмы, обогащенной тромбоцитами (PRP).
Забор крови проводили в вакуумную систему типа Vacuette® с цитратом натрия. Кровь центрифугировали при 1000 об/мин в течение 10 мин, отбирали верхний слой (без эритроцитов) и центрифугировали его при 3600 об/мин в течение 10 мин. Большую часть супернатанта удаляли, осевшие тромбоциты ресуспендировали в оставшейся плазме.
Подготовка ТИК к трансплантации.
В качестве материала-носителя использовали «Остеоматрикс» в виде блоков и костной крошки (ООО «Конектбиофарм»). После отмывания блоков и крошки раствором Хэнкса («ПанЭко») с цефазолином (ОАО «Синтез») (1г/л) на них аккуратно наслаивали PRP, содержащую 7·106 клеток в 1 см3, и по каплям добавляли раствор тромбина («P.Z. Cormay») 50 Ед/мл на 10% растворе хлорида кальция (ОАО «Дальхимфарм») до полимеризации.
Трансплантация ТИК.
Все вмешательства выполнялись в условиях стерильной операционной под местной анестезией. Увеличение высоты альвеолярного отростка в области дна верхнечелюстной пазухи осуществляли по стандартной методике проведения открытого СЛ с доступом к пазухе в области ее передней стенки: проводили горизонтальный разрез по вершине альвеолярного гребня в области отсутствующих зубов; скелетировали альвеолярный отросток; формировали костное «окно» в области передней стенки пазухи до достижения его подвижности; отслаивали слизистую оболочку пазухи и вместе с костным фрагментом смещали ее вверх и внутрь пазухи; образовавшееся пространство в верхнечелюстной пазухе, а также сформированное костное окно заполняли ТИК в виде костных блоков и костной стружки; слизисто-надкостничный лоскут укладывали на место, рану ушивали наглухо.
Имплантация «Bio-Oss».
Интраоперационно остеопластический материал смешивали с аутологичной обогащенной тромбоцитами плазмой, полимеризовали в сгусток и помещали в область дна верхнечелюстной пазухи, как описано выше. Рану ушивали наглухо.
Рентгеновские методы исследования.
Рентгенологическое исследование проводилось на конусном компьютерном томографе «New Tom», интервал среза — 2 мм, а также на цифровом ортопантомографе («ORTHOPHOS XG 5 DS») .
Гистоморфологическое исследование.
Для изучения характеристик костного регенерата через 4 мес после трансплантации проводили гистологическое исследование. Образцы тканей в виде столбиков забирали трепаном диаметром 2 мм, перед формированием ложа для установки дентального имплантата и непосредственно после извлечения фиксировали в 10% нейтральном формалине («Biooptica», Italy) 48 ч. После промывки в проточной воде биопсийный материал декальцинировали в растворе соляной/муравьиной кислоты («Biooptica», Italy) в течение 8 ч. Далее образцы подвергали стандартной гистологической проводке и заливали в парафин («Гистомикс Экстра», Биовитрум). Гистологические срезы получали на микротоме («Leica», Germany) с шагом в 7 мкм. Срезы окрашивали гематоксилином и эозином по Бокку и по Массон—Голднеру. Морфометрический анализ проводился с использованием метода стереоморфометрии [10] в нашей модификации и заключался в определении долей (в %) костной ткани (BV/TV), материала (MatV/TV), рыхло-волокнистой соединительной ткани (RfV/TV), грубоволокнистой соединительной ткани (FbV/TV), ЖТ (FTV/TV) относительно всех тканей в регенерате. Нормальность распределения вариант в группе определялась тестом Шапиро—Вилка. Если распределение вариант соответствовало нормальному, для установления межгрупповых различий применяли однофакторный дисперсионный анализ с последующим тестированием по Ньюману—Кейлсу и t-тестированием (для попарного сравнения данных контрольной и опытной групп). Если распределение вариант в группе не соответствовало нормальному, применяли ранговый дисперсионный анализ Крушкала—Уоллисса с последующим тестированием по Манну—Уитни (для попарного сравнения данных контрольной и опытной групп). Для всех сравнений был выбран 5% уровень значимости.
Результаты и обсуждение
Высота альвеолярного отростка при использовании ТИК ЖТ составляла 0,9—3 мм, при использовании «Bio-Oss» — 1,0—4,8 мм, высота альвеолярного отростка после трансплантации, по данным КТ, — соответственно 10—16 и 9—15 мм.
По данным КТ-исследования, среднее увеличение высоты альвеолярного отростка при трансплантации ТИК ЖТ составило 10 мм, при имплантации «Bio-Oss» — 8 мм, при этом минимальная высота альвеолярного отростка до трансплантации в 1-й группе составляла 0,9 мм, во 2-й — 1,0 мм.
Гистологическое исследование через 4 мес после трансплантации ТИК показало, что костный регенерат состоял преимущественно из частичек зрелой пластинчатой костной ткани, ориентированных в пространстве наподобие балок губчатой кости. Доля костной ткани (BV/TV) — в среднем 46,6%. Межбалочное пространство заполнено на 31% рыхлой волокнистой соединительной тканью (RfV/TV). Среди балок губчатой кости определялись включения материала (MatV/TV) — 2,9%, которые находились в тесном контакте с новообразованной костной тканью и часто были включены в ее архитектонику. Рыхлая волокнистая соединительная ткань (РВСТ) заполняла все межбалочное пространство и содержало значительное количество сосудов. Значительных инфильтративных, гигантоклеточных и воспалительных реакций на материал выявлено не было (рис. 3, 5).
Рисунок 3. Костный регенерат через 120 дней после трансплантации ТИК ЖТ.
Рисунок 5. Соотношение (в %) частей регенерата через 4 мес после трансплантации ТИК ЖТ.
По данным гистологического исследования через 6 мес после имплантации «Bio-Oss», костный регенерат состоял преимущественно из частичек незрелой костной ткани, ориентированных в пространстве по поверхности материала и иногда сливающихся друг с другом. Доля костной ткани (BV/TV) — в среднем 33,6%. Межбалочное пространство было заполнено на 41% грубоволокнистой соединительной тканью (ГВСТ) (FbV/TV). Среди полей фиброзной ткани определялись включения материала (MatV/TV) — 20,7%, которые находились в тесном контакте с новообразованной костной тканью. Было выявлено значительное количество гигантских клеток как вокруг материала, так и в межбалочном пространстве (рис. 4, 6).
Рисунок 4. Костный регенерат через 180 дней после имплантации «Bio-Oss».
Рисунок 6. Соотношение (в %) частей регенерата через 6 мес после имплантации «Bio-Oss».
Для увеличения высоты дна верхнечелюстной пазухи традиционно используют остеоиндуктивные материалы на основе фосфата кальция того или иного происхождения прежде всего потому, что они являются недорогими и эффективными материалами для направленной костной регенерации.
Морфологические исследования, проведенные в отдаленные сроки, показывают, что при имплантации, например, «Bio-Oss» доля костной ткани в среднем колеблется около 30% [4, 12], тогда как при аутотрансплантации она составляет 40—60% [8, 13]. Поскольку для получения аутотрансплантата необходимо дополнительное операционное поле и донорские зоны ограничены, клеточные трансплантаты могут стать достойной альтернативой аутотрансплантатам. Так, при трансплантации живых эквивалентов костной ткани доля костного регенерата сопоставима с таковой при аутотрансплантации [6, 11].
Кроме того, в нашем исследовании были выявлены выраженные различия в течении регенеративного процесса при трансплантации ТИК и имплантации «Bio-Oss». Если межбалочное пространство после трансплантации ТИК в основном было заполнено рыхлой волокнистой соединительной тканью, богатой сосудами, то в образцах после имплантации гидроксиапатита выявлялось значительное количество грубоволокнистой соединительной (рубцовой) ткани, что свидетельствовало о патологической регенерации. Выраженная инфильтрация остеокластами и макрофагами в сочетании со склеротическими изменениями свидетельствовала о негативной реакции организма на остеопластический материал «Bio-Oss».
Перспективы
Сегодня в костной трансплантологии в основном используются аутогенные материалы и БоТП (богатая тромбоцитами плазма). Последняя представляет собой гель, содержащий плазму крови и тромбоциты, играющие основную роль в регенерации и заживлении тканей.
Судя по всему, недалеко то время, когда в распоряжение хирургов поступят аутогенные биоматериалы, выращенные вне организма.
Однако для любых имплантационных материалов, независимо от их происхождения, необходим носитель, обеспечивающий эффективную регенерацию тканей и отвечающий ряду требований, в числе которых:
- высокая адгезия клеток;
- сохранение пространства;
- положительное влияние на морфологию кости;
- поддержка дифференциации клеток.
И с этой точки зрения костные заменители, подобные Био-Осс, способные работать вместе с БоТП, могут рассматриваться как очень перспективные материалы.
Альтернативы наращиванию
Имплантологи клиники «Smile-at-Once» в совершенстве владеют современными методиками дентальной имплантации, поэтому нашим клиентам мы рады предложить протоколы лечения, которые позволяют обойтись без проведения дополнительных процедур наращивания.
Атрофия – это ограничение для проведения лишь двухэтапной имплантации с отсроченной нагрузкой. Если речь идет о восстановлении одного зуба, особенно в зоне улыбки, то наращивание губчатого отдела кости и применение двухкомпонентных имплантов действительно оправдано.
Одноэтапная имплантация с немедленной нагрузкой
Но при отсутствии большого количества зубов, а также при полной адентии наращивание кости по всему ряду, во-первых, будет достаточно дорогостоящей процедурой, во-вторых, чрезмерно сложной и длительной. Именно поэтому в данных ситуациях рекомендуются методы имплантации с немедленной нагрузкой – они позволяют реабилитировать кость и вернуть пациента к полноценной жизни практически сразу.
При данном протоколе используются специально разработанные импланты, которые крепятся как в губчатой кости, так и в базальном отделе, кортикальной пластине, а в ряде ситуаций задействуют скуловую кость и контрфорсы. Они моментально нагружаются протезом, поэтому челюстная кость получает привычную нагрузку и внутри нее запускаются естественные обменные процессы. Нормализуется питание клеток, они получают достаточно количество кислорода, активно разрастаются и ткань восстанавливается. Поэтому атрофия кости в данной ситуации не помеха комфортному и полноценному лечению, а также надежной фиксации имплантов.
Подробнее о технологии одноэтапной имплантации с немедленной нагрузкой >>>
1 Lars Schropp, A. Wenzel, L. Kostopoulos, et al. Bone Healing and Soft Tissue Contour Changes Following Single-Tooth Extraction: A Clinical and Radiographic 12-Month Prospective Study. 2 По материалам портала studopedia.ru. Биохимия костной ткани.
Выводы
Использование в челюстно-лицевой хирургии биоматериалов естественного происхождения становится все более востребованным. Их развитая внутренняя поверхность положительно влияет на адгезию и дифференцирование клеток в зоне дефекта.
Низкая резорбируемость повышает стабильность объема. Естественная, близкая к человеческим структура носителей, создает благоприятные условия для регенерации новых костей. Все это сулит материалам, подобным Био-Осс, высокую востребованность в хирургии.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Теги костные материалы
Понравилась статья? Следите за обновлениями
Предыдущая статья
Обтурация корневых каналов – продление жизни и полноценных функций зубу
Следующая статья
Когда оправдано использование аппарата Персина для коррекции аномалий прикуса
Особенности оперативного вмешательства
Как правило, восстановление кости и установку имплантата осуществляют одновременно. Для формирования новой кости дефект заполняют биоматериалом Био-Осс, а для направленной регенерации на рану накладывают мембрану Био-Гайд.
После проведения оперативного вмешательства возможно появление небольшой припухлости и отечности, которые можно устранить с помощью холодного компресса. Первые 10-14 дней во время чистки зубов следует избегать травм оперированного участка, пользоваться антибактериальным ополаскивателем. При появлении сильных болезненных ощущениях врач может назначить обезболивающее средство. При этом важно регулярно показываться врачу-стоматологу даже в том случае, если ничего не беспокоит и заживление протекает благополучно.